Buch der Synergie

| Blättern |
 TEIL C
TEIL C
ENERGIESPEICHERN
Die verschiedenen Batterie- und Akkumulatorentypen (XVIII)
Thermalbatterie
Thermalbatterien (auch Hochtemperaturbatterien oder Schmelzsalzbatterien genannt)
enthalten im Lagerzustand bei Raumtemperatur nicht leitende, feste
Elektrolyte und sind somit inaktiv. Erst bei hohen Temperaturen (200°C
– 800°C) schmelzen die Elektrolyte (Salze wie Natriumchlorid, Kaliumchlorid
oder Lithiumchlorid), wodurch die über eine hohe Leistungsdichte verfügende
Batterie aktiviert wird.
Die von dem Raketenforscher Dr. Ing. Georg Otto Erb auf Basis von Kalziumchromat entwickelten thermisch aktivierten Batterien werden in Deutschland im Zweiten Weltkrieg u.a. in der V2-Rakete eingesetzt. Nach dem Krieg wird Erb vom britischen Geheimdienst verhört und seine Arbeit in einem Bericht mit dem Titel ,Theorie und Praxis der Thermal-Zellen’ dokumentiert, der anschließend an die Ordnance Development Division des National Bureau of Standards in den Vereinigten Staaten weitergegeben wird. Dort wird die Technologie sofort genutzt, um die lästigen flüssigkeitsbasierten Systeme zu ersetzen, die zuvor für Artilleriezünder verwendet wurden.
Beginnend in den 1970er Jahren werden die Primärzellen dieses Typs bei Anwendungen eingesetzt, bei denen es auf eine sehr lange Lagerfähigkeit und Zuverlässigkeit ankommt, während die Einsatzdauer eher gering ist und nur wenige Sekunden bis Minuten beträgt – d.h. praktisch ausschließlich im militärischen Bereich (Raketen, Atombomben) oder in der Raumfahrt. Hierbei wird der Elektrolyt erst zum Zeitpunkt des Einsatzes der Batterie durch eine pyrotechnische Ladung (Hitzepapier oder Hitzetablette, z.B. Zr-BaCrO4) zum Schmelzen gebracht (ca. 300 – 500°C) und die Batterie dadurch aktiviert.
Ab Mitte der 1960er Jahren wird die Technologie auf ihre Eignung in Elektrofahrzeugen untersucht, da Sekundärzellen dieses Typs wieder aufladbare Akkumulatoren darstellen, wie beispielsweise die Natrium-Nickelchlorid-Batterie oder der Natrium-Schwefel-Akkumulator, die schon separat behandelt worden sind (s.d.). In den 1980er Jahren beteiligen sich auch die Argonne National Laboratories an den Forschungen.

Zu den international aktiven Herstellern der Primärzellen gehört die deutsche Firma Diehl & EAGLE PICHER GmbH in Röthenbach a. d. Pegnitz, deren selbst entwickelte Thermalbatterien mit einem Elektrolyt aus einer anorganischen Salzmischung ihr Einsatzgebiet hauptsächlich in militärischen Programmen (Flugkörper, Flugzeug-Schleudersitze, gelenkte Artilleriegeschosse) und Luft- und Raumfahrt-Anwendungen finden (z.B. Patent DE 19958411).
Als die wesentlichen Stärken werden die lange Lagerfähigkeit praktisch ohne Selbstentladung, die Wartungsfreiheit, die hohe Energiedichte und der schnelle Spannungsanstieg nach der Aktivierung betont, sowie die Fähigkeit, extrem hohen mechanischen Belastungen standzuhalten.
Dem Stand von 2014 zufolge werden 36 verschiedene Modelle mit Spannungen zwischen 2 V und 300 V und Strömen von 1 mA bis 300 A angeboten. Ihre Aktivierung kann elektrisch oder mechanisch erfolgen, bei einer Aktivierungsdauer von 150 ms bis 1 s und einer Einsatzdauer zwischen 10 s bis 60 min. Dabei sollen die Thermalbatterien widerstandsfähig gegen Schock, Vibration, Beschleunigung, Unterdruck und Überdruck sein, und außerdem auch bei einer Umgebungstemperatur zwischen -54°C bis +85°C funktionieren.
Ein weiterer Hersteller ist die französische Firma ASB Group in
Bourges Cedex, die ihre Produkte als ideale Quelle für eine Energiereserve
anpreist. Die Zuverlässigkeit beträgt mehr als 99,95 %, die Batterie
ist für 15 Jahre und länger völlig wartungsfrei, funktioniert auch
unter schwersten äußeren Umständen – und soll die leistungsfähigste
und stärkste auf dem Markt sein.

Einer Veröffentlichung vom November 2002 zufolge arbeitet ABS mit der schottischen Firma Missiles and Space Batteries (MSB) in Coatbridge zusammen, wobei Thermalbatterien für Luftfahrtanwendungen entwickelt und in Serie hergestellt werden. Die Packs bestehen aus jeweils 4 Batterien (wobei eine kleine drei größere aktiviert), die 240 A über 180 Sekunden oder 25 A über 1.200 Sekunden liefern können. Produziert werden ca. 30.000 Stück pro Jahr. MSB hatte schon in den davor liegenden 5 Jahren Thermalbatterien als Notstromsysteme für Militärflugzeuge hergestellt.
Im Juni 2006 bezeichnet sich ASB als europäischer Marktführer im Bereich der Thermalbatterien und berichtet stolz von einer neuentwickelten Reihe mit sehr kleinen Abmessungen, die unter den Namen ,SMART Batteries’ bei der neuesten Smart- Munition der Artillerie eingesetzt werden. Gleichzeitig wird in Cockeysville, Maryland, die US-Tochtergesellschaft Advanced Thermal Batteries Inc. (ATB) gegründet, welche die lokalen Aktivitäten der im April dieses Jahres übernommenen Saft America Inc. weiterführt. Ebenfalls mit dabei ist die EADS Inc. (später Airbus Group).
Dies geschieht sehr erfolgreich, aber ohne viel Presse, da die Geschäfte ausschließlich mit führenden US-Rüstungsunternehmen erfolgen. Meldungen vom Juni 2011 zufolge wird ATB ein neues Dünnfilm-Beschichtungsverfahren zur Herstellung von thermischen Batterien für Kernwaffen und Munition, das an den Sandia National Laboratories erfunden wurde, industrialisieren. Sandia hat seit 1975 etwa 30 Thermobatterie-Designs entwickelt.
Das Beschichtungsverfahren könnte für ausgewählte thermische Batterien verwendet werden, die in den thermonuklearen B61 Waffen ersetzt werden, als Teil eines Lebensverlängerungsprogramms, mit dem Sandia beauftragt ist. Das Projekt, die größte Waffen-Sanierung im US-Atomwaffen-Komplex, soll im Jahr 2017 beginnen. Im November 2013 meldet ATB einen Multi-Millionen-Dollar-Auftrag von der Lockheed Martin Co. für die Qualifizierung eines thermischen Batteriesystems.
Ultra-Batterie
Der
Begriff Ultra-Batterie ist
ein der Presse entnommener provisorischer Name - bis die hier beschriebene
neue Technologie eine allgemein gültige Bezeichnung erhält, möglicherweise Xenondifluorid-Batterie.
Im Juli 2010 stellt der Chemiker Choong-Shik Yoo von der Washington State University in Pullman zusammen mit Kollegen das Konzept eines neuen Verfahrens zur Speicherung von Energie vor, bei dem die Edelgasverbindung Xenon(di)fluorid (XeF2) unter Druck gesetzt wird – eine der wenigen chemischen Verbindungen des Edelgases Xenon, die einigermaßen stabil ist. Die farblos-transparente, kristalline und sehr leicht flüchtige Verbindung, in der jeweils ein Xenon- mit zwei Fluoratomen verbunden ist, wird als starkes Oxidations- und Fluorierungsmittel in der organischen Synthese verwendet und gilt als brandfördernd und sehr giftig (a).
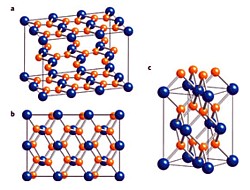
In einer sogenannten Diamantstempelzelle wird der Druck auf 100 Gigapascal erhöht, was etwa eine Million Mal so viel ist, wie an der Erdoberfläche herrscht, und mit dem Druck zu vergleichen ist, der auf der Hälfte des Weges zum Erdkern auftritt. Dabei verkleinern sich die Abstände zwischen den Molekülen stark. Die Druckkammer im Kleinformat hat den Vorteil, daß die beiden druckausübenden Stempel – wie der Name schon sagt – aus Diamant bestehen und damit auch lichtdurchlässig sind. Auf diese Weise läßt sich die komprimierte Probe untersuchen, ohne daß der Druck entfernt werden muß. Die damit erreichbare extrem hohe Energiedichte im komprimierten Material wird nur noch von der in Atomkernen vorherrschenden übertroffen.
Im Fall des Xenondifluorids beobachten die Wissenschaftler eine erstaunliche Verwandlung: Aus dem weißen Kristall, der keinen Strom leiten kann, wird bei einem Druck von um die 50 Gigapascal – etwa dem 500.000-fachen des Atmosphärendrucks – ein rötliches, zweidimensionales Material (XeF4), das entfernt an Graphit erinnert (b). Wie diese Kohlenstoffvariante ist auch das zusammengepreßte Xenonfluorid aus Schichten aufgebaut, in denen jedes Xenonatom nicht mehr mit zwei, sondern jetzt mit vier Fluoratomen gekoppelt ist.
Bei weiter steigendem Druck über 70 Gigapascal verändert sich die Bindungen der Moleküle jedoch noch weiter, worauf eine metallische, schwarze, dreidimensionale Netzwerkstruktur entsteht, bei der nun jedes Xenonatom von acht Fluoratomen umgeben ist (XeF8) (c).
Die Wissenschaftler weisen darauf hin, daß es sich bei ihrer Ultra-Batterie, die mehr Energie speichert als jede andere bisher bekannte Batterie, noch um Grundlagenforschung handelt. Sie sind aber überzeugt davon, daß eine große Menge der mechanischen Energie, die zum Aufbau des Drucks benötigt wird, in Form von chemischer Energie in den Molekülbindungen gespeichert wird und sich von dort auch wieder freisetzen läßt. Bis zu einem praktischen Einsatz als hocheffektiver Energiespeicher wird es allerdings noch dauern.
Finanzielle Unterstützung für die Forschung kommt von der Defense Threat Reduction Agency des US-Verteidigungsministeriums sowie von der National Science Foundation.
Urin-,
Bio- und Wasserbatterien
Unter diesem Titel fasse ich eine Reihe von Entwicklungen zusammen,
die auf organischen Flüssigkeiten wie Blut oder Urin, auf Wasser
oder auf biologischen Materialien wie Algen oder
Schlammbakterien u.ä. basieren. Einige dieser Technologien
sind bereits im Kapitel Micro
Energy Harvesting beschrieben worden (s.d.) - wobei es allerdings
auch mehrere Überlappungen gibt.
Die 1986 gegründete Firma Magnevolt Inc. in
Clayton, North Carolina, verkauft wasserbetriebene Batterien an
die US-Streitkräfte und bezeichnet sich als der weltweit führende Anbieter
von Wasser-aktivierten Qualitäts-Batterien. Grundlage ist eine eigens
entwickelte Magnesium-Silberchlorid-Batterie,
die in Süßwasser betrieben wird. Eine weitere Batteriechemie basiert
auf Kupferchlorid-Magnesium.
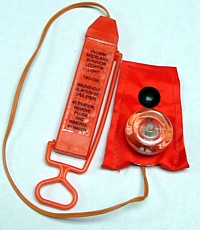
Die beiden Chemien unterscheiden sich in den verwendeten Materialien, gleichen sich ansonsten aber in vieler Hinsicht: beide nutzen Trockenelemente in der Batterie, ohne daß es einen Elektrolyt gibt, bis sie in das Wasser eingetaucht wird, wobei dieses sowohl Salz- als auch Süßwasser sein kann. Die Batterien können für Jahre gelagert werden und lassen sich in Millisekunden aktivieren. Solange sie versiegelt bleiben, haben sie eine unbestimmte Haltbarkeit. Wasseraktivierte Batterien sind natürlich ,One-Shot’-Batterien, weil die chemische Reaktion, welche die Spannung liefert, nicht umkehrbar ist.
Dem Stand von 2014 zufolge bietet das Unternehmen über 10 verschiedene Batteriemodelle mit Silberchlorid sowie 8 mit Kupferchlorid an, außerdem fertigt es verschiedene Ausführungen der ,Survivor Locator Lights’, die an Schwimmwesten befestigt acht Stunden lang Strom für ein Signallicht liefern, sobald sie durch Entfernen eines Handgriffs und Eintauchen ins Meerwasser aktiviert werden.
Der Chemiker Adam Heller entwickelt Ende 2002 gemeinsam
mit weiteren Forschern der University of Texas in
Austin eine Kleinst-Batterie, die Ihre Energie aus der Körperflüssigkeit
von Menschen bezieht. Die auch als Bio-Brennstoff-Zelle bezeichnete
Apparatur bezieht ihre Energie aus der Reaktion von Sauerstoff mit
Zucker.
Dabei werden zwei mit Enzymen überzogene Kohlenstoff-Fasern in den Körper implantiert, wo sie dem Zucker Elektronen entreißen und diese auf den Sauerstoff übertragen, so daß ein elektrischer Strom fließt. Bei einer Körpertemperatur von 37ºC und einem pH-Wert von 7,2 erreicht die Batterie eine Leistung von ca. 1,9 µW. Damit eignet sie sich zwar schon zur Überwachung des Blutzuckerspiegels bei Diabetikern, aber noch nicht für höheren Energiebedarf wie bei z.B. dem Antrieb eines künstlichen Herzens.
Im November 2003 berichtet die Presse, daß Larry Kostiuk
an der University of Alberta in Kanada an einer mit
Wasser betriebenen Batterie arbeitet, deren besondere Eigenschaft die
direkte Stromproduktion aus Wasser auf der kleinsten Skala ist. Sie
ist unter ihrem Namen ,elektrokinetische Batterie’ im Kapitel Micro
Energy Harvesting (Strömungen) beschrieben worden (s.d.).
Das Institute of Bioengineering and Nanotechnology in
Singapur gibt im August 2005 bekannt, daß man eine
Batterie entwickelt habe, die mit Urin funktioniert.
Die papierdünne Batterie liefert mit einem einzigen Tropfen Urin (0,2
Milliliter) eine elektrische Leistung von mehr als 1,5 mW und soll
einfachere und schnellere Krankheitsdiagnosen ermöglichen: Der Urin
dient als Energiequelle und wird gleichzeitig analysiert, etwa um die
Glukosekonzentration zu bestimmen.
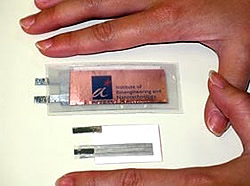
Die Batterie besteht aus einer Schicht Filterpapier, das in Kupferchlorid getaucht und zwischen einen Magnesium- und einen Kupferstreifen geklemmt wird. Nach dem Trocknen wird das Batterie-Sandwich in Plastikfolie eingeschweißt, um ein Verschieben der einzelnen Bestandteile zu verhindern.
Das Funktionsprinzip der Batterie ist einfach: Wird ein Tropfen Urin auf die Batterie gegeben, wird er vom Papier aufgesaugt. Das Kupferchlorid löst sich und reagiert mit dem Magnesium, wobei Strom erzeugt wird. Die Urinbatterie soll Biochips von Kreditkartengröße ermöglichen, die nach einmaliger Verwendung problemlos entsorgt werden können. Nach etlichen Verbesserungen liefert ein neuer Prototyp mit einem Tropfen Urin bereits 1,5 V – und das 90 Minuten lang. Das neue Modell funktioniert auch mit anderen Körperflüssigkeiten wie Tränen, Blut oder Sperma.
Ende 2006 präsentiert der japanische Erfinder Susumu
Suzuki, Präsident des Tokyoter Baustoff-Herstellers Total System
Conductor (TSC), eine Wasser-Batterie, die
genauso stark ist wie ein Standard-Mangan-Dioxid-Batterie und in erster
Linie aus Kohlenstoff-Materialien besteht. Der Feuchtigkeitsbedarf
sei sehr gering, schon daran zu lecken würde ausreichen, um einige
Miliampere zu erzeugen.
Bei einer Großproduktion soll sie nur ein Zehntel des heutigen Preises vergleichbarer Batterien kosten. Interessant ist die Batterie insbesondere dadurch, daß sie in trockenem Zustand fast unbegrenzt haltbar ist. Damit bietet sie sich als das ideale System für Notfälle an, da es bei Bedarf ausschließlich etwas Wasser benötigt, um aktiviert zu werden.

Im September 2007 kommt in Japan unter dem Namen NoPoPo (Non-Pollution Power) eine weitere Urin-Batterie auf den Markt, die aus Magnesium und Kohlenstoff besteht und 500 mhA leistet.
Mit einer kleinen Pipette läßt sich die 1,5 V AA oder AAA Zell 3 – 5 Mal wieder aufladen, indem etwas Wasser oder andere Flüssigkeiten hineingeträufelt werden, wie Bier, Sake, Cola oder sogar Urin. Im April 2008 präsentiert der Hersteller Aqua Power System Japan aus Tokio seine Batterie erstmals auf der Hannover Messe.

Obwohl das Produkt nicht dieselbe Energiedichte hat, wie eine übliche Alkaline Batterie, ist es für elektronische Geräte dennoch sehr gut geeignet. Bereits im Juni 2009 wird eine knapp 10 cm lange Lampe namens NoPoPo Mini Lantern für 40 - 50 $ angeboten, die sich mit einer Handbewegung von einer Tisch- zu einer Taschenlampe verwandeln läßt.
Solange die Lampenbatterie nicht durch eine Flüssigkeit aktiviert wird, kann sie ihre Ladung bis zu zehn Jahre lang in Reserve halten. Inzwischen scheint es die Firma aber nicht mehr zu geben, zumindest ihre Homepage ist tot.
Ähnliche Produkte sind ein 8-stelliger Taschenrechner aus biologisch abbaubarem Kunststoff für ca. 14 $, dessen Wasserzelle genug Energie für drei bis sechs Monate liefert, sowie verschiedene Uhren und Wecker.
Der Biophysiker Simon Rock Levinson von der University of Colorado
in Denver stellt im Dezember 2007 eine Biobatterie
vor, die darauf basiert, daß lebende Zellen Ionen durch ihre Membran
pumpen, was eine Potentialdifferenz erzeugt und somit ausgenutzt
werden kann, um Strom zu machen. Eine derartige Batterie ist ideal
für die Versorgung von implantierten Geräten wie Insulinpumpen oder
Herzschrittmacher, weshalb sie auch sogleich patentiert wird (EP-Nr.
2035539 bzw. US-Nr. 20090196902).
Speziell Nierenzellen, die Ionen besonders gut transportieren,
sind geeignet, eine solche Miniatur-Batterie herzustellen, die durch
das Stapeln einer großen Anzahl von Zellschichten gebildet wird, um
die Spannung und den Strom, den sie erzeugt, zu steigern. Die Zellkultur
kann Sauerstoff und Nährstoffe aus der Blutbahn des Wirts ziehen. Werden
die Monoschichten gar aus sich unbegrenzt vermehrenden Zellen hergestellt,
kann die Biobatterie solange funktionieren, wie der Wirt lebt.
Im Oktober 2008 präsentiert Prof. Chungpin Hovering
Liao von der National Formosa University in Taiwan
die seiner Meinung nach weltweit erste Bio-Batterie auf Grundlage von
Chlorophyll,
die mit jeder Flüssigkeit, so auch Urin, betrieben werden kann.

Um die Batterie zu starten, braucht es nicht viel Zeit: Innerhalb von 10 Sekunden, nachdem der Akku mit Flüssigkeit übergossen wurde, beginnt die zwei- bis fünftägige Stromproduktion – bislang allerdings nur mit der Hälfte der Leistung einer herkömmlichen Batterie.
Die Chlorophyll-Batterie kann fünfmal wieder aufgeladen werden und besitzt eine Gesamtausgangsleistung über ihre Lebensdauer von ungefähr 150 mAh.
Besonders positiv schlagen die potentiell sehr niedrigen Produktionskosten von 3 – 6 US-Cent sowie die völlige Freiheit von toxischen Substanzen zu Buche.
Der auch am Massachusetts Institute of Technology beschäftigte Liao beantragt nun Patente in Taiwan und den Vereinigten Staaten (US-Nr. 20120148915).
Ich habe schon mehrfach die sogenannten Obst- oder
Gemüsebatterien erwähnt, die aus den entsprechenden
Grundschul-Experimenten eigentlich allgemein bekannt sein sollten.
Am verbreitetsten sind vermutlich jene Batterien, der denen man verschiedene
Metallnägel in eine Zitrone oder eine Kartoffel steckt, um sofort eine
Spannung zu erzielen.

Im
Dezember 2008 wird in den Fachblogs eine Uhr präsentiert,
die mit einer aufgeschnittenen Zitrone eine Woche
lang läuft.
Das schlichte Design der Citrus-Clock stammt von Florian Dussopt und Julie Girard aus dem Anna Gram Studio und soll mit der Energie der Frucht, deren Hälften auf die Elektroden aus Zink und Kupfer gesteckt werden, für eine Woche oder länger laufen.
Weitere Beispiele dieser Technologie werden im Kapitel Micro Energy Harvesting behandelt (s.d.).
Im August 2007 meldet die Presse, daß auch Sony die
mobile Stromversorgung mittels einer Bio-Batterie ökologisch verträglich
machen will, in der Zucker und Kohlenhydrate Energie
erzeugen, ähnlich wie bei der Licht-nutzenden Photosynthese.
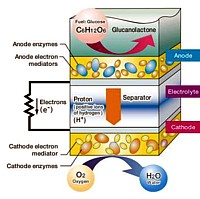
(Grafik)
Erste Testbatterien, die mit einen zuckerhaltigen Fitness-Drink gefüttert werden, leisten bis zu 50 mW. Der Konzern will den Prototyp seiner biologisch abbaubaren Zuckerbatterie nun weiterentwickeln, gleichzeitig prüft er die Möglichkeiten einer breiteren Anwendung, da die zur Herstellung der Batterien benötigten Kohlenhydrate überall leicht aus Pflanzen gewonnen werden können.
Rein theoretisch können die Bio-Batterie mit einem Blatt Papier in DIN A4 Größe bis zu 18 Wh Strom erzeugen, was etwa der Energiemenge entspricht, die durch 6 AA Akkus geliefert werden kann. Im Jahr 2010 teilt das Unternehmen allerdings mit, das der mit Zucker betriebene Akku in der Lage sei, je Quadratzentimeter nur 10 mW Energie zu liefern.

Öffentlich vorgestellt wird die neue Batterie, die ihre Energie aus Papier und einem Enzym gewinnt, im Rahmen der Eco Products Messe in Tokio im Dezember 2011.
Die Bio-Batterie nutzt das Enzym Cellulase, um aus Papier, durch Zersetzung der Zellulose, innerhalb weniger Minuten Glukose (Zucker) zu gewinnen, die im Anschluß dem Bio-Akku als Energiespender dient. Die als Katalysator eingesetzte Cellulase läßt sich dabei mehrfach wiederverwenden. Dies ist der gleiche Mechanismus, mit dem Holz fressende Termiten an ihre Energie kommen.
Aktuell hat Sony die Dicke des Bio-Akkus verringert und zeigt eine Musik-Grußkarte, bei welcher die Musik zu spielen beginnt, sobald der Akku mit Cola oder Orangensaft beträufelt wird. Genaue Angaben zur tatsächlichen Leistung macht das Unternehmen bislang nicht.
Ein Team der Universität Uppsala in Schweden um Prof.
Maria Strømme arbeitet Meldungen vom September 2009 zufolge
am Ångström Laboratory an einem neuartigen Batterietyp, der auf einer
speziellen Art von Zellulose basiert, die von der
weit verbreiteten Cladophora-Alge produziert wird
und bislang eher dafür bekannt ist, an Stränden üble Gerüche zu verursachen.
Diese Technologie ist bereits unter Papier-Batterie präsentiert
worden (s.d.)
Quallen sind allerdings nicht die einzigen Meerestiere, die ausgenutzt
werden können, um Energie zu erzeugen. Adrian Fisher, Paolo Bombelli
und ihre Kollegen an der University of Cambridge entwickeln
ein biophotovoltaisches Gerät, das auf Basis von Algen und photosynthetischen
Bakterien funktioniert, wie im Oktober 2009 berichtet
wird.
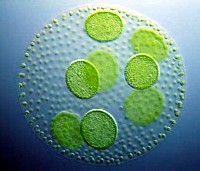
Dabei wird eine transparente, leitfähige Elektrode mit einem Film aus Photosynthesezellen beschichtet, der eine mit Platin-Nanopartikeln besäte Kohlenstoff-Kathode gegenüber steht. Bei Sonneneinstrahlung beginnen die Algenzellen mit der Spaltung von Wasser und der Herstellung von Sauerstoff, Elektronen und Protonen. Diese werden in der Regel von den Algen dazu verwendet, um Kohlendioxid in organische Verbindungen umzuwandeln, doch das neue Gerät leitet sie ab, um Strom zu erzeugen, wobei die Algenzellen die Elektronen sehr großzügig produzieren, wie berichteet wird.
Als Machbarkeitsnachweis zeigt das Team ein Gerät, das eine Uhr versorgen kann. Die Vorrichtung wandelt Sonnenlicht gegenwärtig allerdings nur zu 0,1 % in Elektrizität um, weshalb ein Screening der verschiedenen Algenarten nun den produktivsten Elektronendonor finden soll, um mehr Strom zu produzieren.
Eine hohe Motivation dazu besteht – schließlich könnten Algenzellen auf dem Meer schwimmen und Strom aus Sonnenlicht und Meerwasser erzeugen, ohne Platz (an Land) zu benötigen, was die geringere Effizienz im Vergleich zur konventionellen Photovoltaik zumindest teilweise kompensieren könnte.
Die bisherigen Mittel des Engineering and Physical Sciences Research Council (EPSRC) von rund 160.000 £ werden nun auf 1,6 Mio. £ aufgestockt, um weitere drei Jahre der gemeinsamen Arbeit der Cambridge-Wissenschaftler und eines Teams der Bath University zu finanzieren.
Ebenfalls im Oktober 2009 meldet die Presse, daß ein
Team der Harvard University eine mikrobielle Brennstoffzelle
bzw. Bio-Batterie entwickelt hat, die ausschließlich mit Bodenbakterien betrieben
wird. Über diese Microbial Fuel Cell (MFC) habe ich bereits im Kapitel Micro
Energy Harvesting unter Biomasse berichtet (s.d.).
Interessanterweise wird die MFC vom TIME Magazine bald darauf zu den ,Top 50 Inventions of 2009’ gezählt – allerdings als Entwicklung eines Teams um Leonard Tender vom Office of Naval Research, das nun gemeinsam mit Wissenschaftlern der University of Massachusetts in Amherst die Untersuchung der Mikroorganismen zur Stromerzeugung fortführen will. Die bislang vielversprechendste Entdeckung namens Geobacter wurde im Potomac gefunden, sie könnte der Schlüssel zum Verständnis der mikrobiellen Energieumwandlung sein.
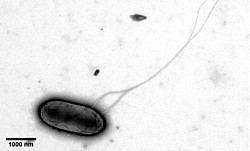
Der Mikroorganism verwendet Pili genannte, haarähnliche Fortsätze, um Strom aus Schlamm und Abwasser zu erzeugen. Die Forscher haben bereits einen neuen Stamm des Geobacter entwickelt, der bei der Herstellung von Strom acht Mal effizienter als andere Stämme ist.
Bei meiner Recherche stelle ich fest, daß es bereits Veröffentlichungen vom März 2003 gibt, die sich mit der Stromproduktion durch Geobacter sulfurreducens beschäftigen, welche direkt an Elektroden angebracht sind. Diese stammen von Daniel R. Bond und Derek R. Lovley an der Michigan State University, die sich für die Unterstützung ihrer Forschungen beim Office of Naval Research, dem Defense Sciences Office der DARPA, dem Office of Science und dem DOE bedanken.
Im Juli 2010 wird Dr. Ioannis Ieropoulos am Bristol
Robotics Laboratory (BRL), einem Projekt der Bristol
University und der University of the West of England,
mit einem Career Acceleration Fellowship Grant des Engineering and
Physical Sciences Research Council (EPSRC) im Wert von 564.561 £ ausgezeichnet,
um im Rahmen eines vierjährigen Projekts zu erforschen, wie Abfall
durch mikrobielle Brennstoffzellen dazu verwendet werden könnte, Energie
zu erzeugen.

Forscher des BRL haben zu diesem Zeitpunkt schon mehrere Jahre, ebenfalls vom EPSRC finanziert, in die Entwicklung mehrerer Versionen des EcoBot gesteckt - eines Roboters, der sich durch Verdauen von Abfall energetisch selbst versorgt. Auch darüber habe ich bereits unter Micro Energy Harvesting berichtet (s.d.).
Nun wird Ieropoulos mit seinem Team das Konzept der MFCs auf die nächste Ebene führen, indem diese zu Stapel verbunden werden – als eine Reihe von Zellen, die sowohl elektrisch als auch in Bezug auf die Flüssigkeitszufuhr-Leitungen über ein Durchflußsystem miteinander verbunden sind. Ein Stapel verbundener MFCs wird viel effizienter und auch mehr Energie erzeugen als die gleiche Anzahl von Einzel-MFCs. Ein wesentlicher Aspekt der Forschung wird es sein, die Verwendung von Urin als Abfallmaterial zu untersuchen, das verwendet werden könnte um die MFCs zu betreiben.

Tatsächlich kommt die Urin-Batterie des BRL im Juli 2013 sehr weit in die Presse, die nun als Entwicklung angepriesen wird, um in Notfallsituationen wie auch in Entwicklungsländern Strom für kleine Geräte zu liefern. Die Ausbeute des Prototyps reicht bereits für einen kurzen Anruf oder eine SMS – und es sei auch das erste Mal, daß Urin real Strom für ein Mobiltelefon geliefert habe. Was natürlich äußerst medienwirksam ist.
Bei dem Experiment werden 12 Keramikzylinder von jeweils gut 10 cm Länge verwendet, die jeweils mit einer Kathode und einer Anode verdrahtet und in Dreiergruppen als Kaskaden gestapelt sind. Der Urin wird in den ersten Zylinder jeder Kaskade eingeführt, wo die Organismen daraus Strom erzeugen. Dies wird im zweiten und dann im dritten Zylinder wiederholt, bevor der ,entladene’ Urin in eine Abfallflasche wandert. Da die Ausgangsleistung der drei Zylinder sehr klein ist, werden vier Kaskaden zusammengeschaltet, was genügend Strom produziert, um einen Handy-Akku aufzuladen.
Da die mikrobiellen Brennstoffzellen in ihrem derzeitigen Entwicklungsstadium allerdings noch immer nicht genug Strom für einen weitreichenden wirtschaftlichen Einsatz liefern, soll das Verfahren auch in den kommenden Jahren weiterentwickelt werden. Ein Teil der Mittel für diese Arbeit kommt von der Bill-und-Melinda-Gates-Stiftung sowie dem Technology Strategy Board.
Im August 2010 präsentiert eine Gruppe von Forschern
der University of Utah auf dem 240. Nationaltreffen
der American Chemical Society einen Brennstoffzellen-Akku, der sich
mit Zucker aus
Soda-Getränken oder sogar aus Pflanzenöl betreiben läßt.
Die ersten Modelle sind recht klein und werden mit Mitochondrien hergestellt, die sich von Glukose aus Nahrungsmitteln ernähren, wie sie in zuckerhaltigen Getränken und Pflanzenölen in besonders hoher Konzentration vorliegt.
Das von der National Science Foundation finanzierte Team geht davon aus, das erste zu sein, dem es gelungen ist eine Brennstoffzelle mit einer körpereigenen Energiequelle zu machen, da es das erste derartige Gerät ist, das auf einem der mikroskopischen Teile der Milliarden von Zellen in unserem Körper basiert. Mitochondrien fungieren dort u.a. als Energiekraftwerke, indem sie das energiereiche Molekül Adenosintriphosphat bilden.
Daß auch Aequorea victoria Quallen, die im
Dunkeln leuchten, die Zutaten für eine neue Art von Brennstoffzellenakku
enthalten, berichten Wissenschaftler um Zackary Chiragwandi an der Chalmers
University of Technology in Göteborg, Schweden, im September 2010.

Das Leuchten dieser Tiere wird durch das grün fluoreszierendes Photoprotein Aequorin produziert (Green Fluorescent Protein, GFP). Über dessen Einsatz zur Entwicklung neuartiger Solarzellen habe ich schon im Kapitel über die nanokristallinen Farbstoffzellen berichtet.
Die schwedischen Forscher plazieren einen Tropfen GFP auf Aluminium-Elektroden, wo es sich selbst zu Strängen verknüpft. Sobald das Ganze mit UV-Licht bestrahlt wird, absorbiert das Photoprotein die Photonen und emittiert Elektronen, womit es einen Strom erzeugt.
Die gleichen Proteine werden nun verwendet, um eine biologische Brennstoffzelle herzustellen, die sogar ohne externe Lichtquelle Strom macht. Anstelle dieser Lichtquelle wird eine Mischung aus Magnesium- und Luciferase-Enzymen verwendet, wie sie in Glühwürmchen (Lampyridae) und Seefedern (Renilla reniformis) zu finden sind, um Strom aus dem biophotovoltaischen Gerät zu generieren.
Im gleichen Monat wird aus der University of Texas at Austin (UTA)
vermeldet, daß die Chemieprofessoren Christopher Bielawski und Jonathan
Sessler in Zusammenarbeit mit weiteren Kollegen und Studenten zwei Moleküle geschaffen
haben, die sich treffen und Elektronen austauschen können, ohne sich
dabei zu vereinen, um eine neue Verbindung zu bilden, wie es bei den
bestehenden elektrochemischen Zellen der Fall ist.
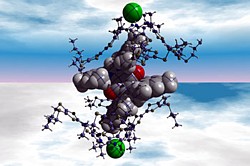
Diese Moleküle werden wirkungsvoll federbelastet, um wieder auseinander zu streben, nachdem sie miteinander interagiert haben. Nachdem der Elektronentransfer stattfindet, bilden sich zwei positiv geladenen Moleküle, die sich gegenseitig abstoßen, ähnlich wie Magnete einander abstoßen, wenn sie in einer bestimmten Weise gehalten werden. Damit wird ein chemischer Schalter installiert, der es dem Elektronentransferprozeß erlaubt, auch in entgegengesetzter Richtung zu verlaufen.
Auf der Abbildung ist ein zusammengesetzter Satz von verschiedenen Molekülen zu sehen, die sich treffen, Elektronen auszutauschen, und sich dann zerlegen, weil Chloridionen (grüne Kugeln) vorhanden sind. Sobald man diese Chloridionen entfernt, kann der gesamte Vorgang umgekehrt werden. Der nächster Schritt soll nun zeigen, ob diese Prozesse auch in einer kondensierten Phase, wie in einem Film, auftreten, und nicht nur in einer Lösung.
Sessler zufolge sie dies das erste Mal, daß das Vorwärts- und Rückwärtsschalten des Elektronenstroms über einen Schaltvorgang auf molekularer Ebene erfolgt ist. Das Verständnis der Elektronentransferprozesses in diesen Molekülen gibt den Forschern wichtige Hinweise zum Entwurf einer effizienten organischen Batterie, denn ein derartiger ,Elektronenschalter’ kann dünne, leichte und leistungsstarke Akkus zur Realität werden lassen, die keinerlei giftigen Schwermetalle mehr benötigen.
Darüber hinaus könnte der molekulare Schalter auch einen Schritt in Richtung der Technologie bedeuten, welche die Fähigkeit der Pflanzen imitiert, Licht zu ernten und durch Photosynthese in Energie zu verwandeln (s.d.). Mit solch einer Technologie könnte Kraftstoff direkt aus der Sonnenenergie erzeugt werden, anstatt durch eine (Bio-Treibstoff) Pflanze als Mittler.
Im November 2010 berichtet die Fachpresse von zwei
Forscherteams des Centre national de la recherche scientifique (CNRS)
in Amiens, Frankreich, deren Ziel die Entwicklung eines organischen
Lithium-Akkus ist, der organische, aus der Landwirtschaft
zurückgewonnene Rohstoffe verwendet und zu einem
späteren Zeitpunkt zur Marktreife gebracht werden soll. Die grundlegende
Idee besteht darin, nicht nachwachsende Rohstoffe durch organische
zu ersetzen.
Das Recycling und die Beseitigung dieser Batterien würde durch die verwendeten organischen Materialien deutlich vereinfacht, da diese oft brennbar sind. Am Ende ihres Lebenszyklus gibt die ,pflanzliche’ Batterie das eingespeiste Kohlendioxid als Wärme ab, während das enthaltene Lithium vollständig wiederverwertet wird.
Daß sich auch malaysische Wissenschaftler um Prof. Dino Isa von der University
of Nottingham Malaysia Campus (UNMC) mit der Nutzbarmachung
der biologischen Vielfalt ihres Landes befassen, um alternative Rohstoffe
für High-Tech-Produkte wie Elektrofahrzeug-Batterien zu finden, ist
im Februar 2011 zu erfahren.

Dabei entdecken sie, daß Bambus, Kokosnuß-Schalen und die Schalen der Durian-Frucht in eine aktivierte Form des Kohlenstoffs umgewandelt werden können, die zur Herstellung von Komponenten elektrischer Batterien und Superkondensatoren geeignet ist. Die bislang eingesetzte Aktivkohle wird in der Regel aus Steinkohle gemacht, doch nun könnte sie aus einer natürlichen, erneuerbaren Quelle bezogen werden, was die Materialkosten zur Herstellung der Batteriekomponenten um bis zu 30 % zu reduzieren vermag.
Diverse tropische Früchte bilden deshalb sehr gutes Ausgangsmaterial, weil sie viele Poren haben, womit es mehr Fläche für den Ladungerhalt gibt, was wiederum die Speicherfähigkeit des Superkondensators erhöht.
Das Verfahren zur Beschaffung oder Kultivierung der Pflanzenerzeugnisse und ihre Umwandlung in Aktivkohle könnte dabei als Hausindustrie ausgelagert werden, was der ländlichen Bevölkerung ein zusätzliches Einkommen verschafft. Auch sind die Pflanzen in der tropischen Nation ohne weiteres verfügbar, was eine nachhaltige und umweltfreundliche Beschaffung bzw. Bewirtschaftung erlaubt.
Die UNMC und ihr Partner Shaz Holdings starteten bereits im Januar eine Pilotanlage, um die ,grünen’ Superkondensatoren zu produzieren, und hoffen nun, in etwa fünf Jahren eine Fabrik zur Großserienproduktion eröffnen zu können.
Im Mai 2011 veröffentlicht ein großes Wissenschaftler-Team
der University of East Anglia in England einen Bericht,
der die Entwicklung von praktikablen mikrobiellen Brennstoffzellen
einen großen Schritt vorwärts bringen könnte. Die Forscher, die gemeinsam
mit Kollegen des Pacific Northwest National Laboratory in
Richland, Washington, arbeiten, melden nämlich, daß sie die genaue
molekulare Struktur der Proteine entdeckt haben, die
es bakteriellen Zellen ermöglichen, elektrische Ladung zu übertragen
(,Structure of a bacterial cell surface decaheme electron conduit’).
Mit diesem Wissen kann nun die Arbeit an Techniken beginnen, um Bakterien direkt mit Elektroden zu verbinden, was zu viel effizienteren mikrobiellen Brennstoffzellen führen könnte – die auch als Bio-Batterien bezeichnet werden.
Das Team verwendet die Röntgenkristallographie, um die Struktur der elektronenübertragenden Proteine zu bestimmen, die an der Oberfläche einer Shewanella oneidensis Bakteriumzelle angebracht wurden. Dabei machen sie Fortschritte im Verständnis, wie einige Bakterienarten Elektronen von der Innen- zur Außenseite einer Zelle bewegen. Den Forschern zufolge bildet die Ermittlung der genauen molekularen Struktur der an diesem Prozeß beteiligten Schlüsselproteine einen entscheidenden Schritt zur Erschließung von Mikroben als eine tragfähige Stromquelle der Zukunft.
Neben den Folgen für die Brennstoffzellen-Technologie könnte die Entdeckung auch bei der Entwicklung der Mikroben-basierten Mittel helfen, die zum Reinigen von Öl- oder Uran-Verschmutzungen genutzt werden. Was vermutlich auch ein Grund dafür ist, daß das Projekt vom Biotechnology and Biological Sciences Research Council (BBSRC) und dem US-Energieministerium finanziert wird.
Ein Durchbruch wird dann im März 2013 gemeldet. Die Ergebnisse der Wissenschaftler zeigen, daß auch Bakterien, die direkt auf Metall- oder Mineraloberflächen liegen, eine elektrische Ladung durch die Zellmembranen übertragen können. Dies bedeutet, daß es möglich ist, Bakterien direkt an Elektroden ,anzubinden’ - was die Herstellung einer effizienten mikrobiellen Brennstoffzelle oder Bio-Batterie einen Schritt näher bringt.
Mit Unterstützung der National Science Foundation beschäftigt sich
auch ein Team der Penn State University um den Umweltingenieur
Bruce Logan mit der Entwicklung mikrobieller Brennstoffzellen, die Bakterien enthalten,
welche kommunales Abwasser in Energie umwandeln können.

Der Meldung vom August 2011 zufolge werden in den USA 5 % des Stroms für den Betrieb der Wasser-Infrastruktur verwendet. Ein Anteil davon könnte gewonnen werden, indem das Abwasser buchstäblich in diese Art von Brennstoffzellen gegossen wird, wo die Bakterien die organischen Abfälle fressen und als Nebenprodukt Elektronen abgeben, welche von Kohlenstoff-Borsten in der Brennstoffzelle eingesammelt werden. Logan präsentiert einen kleinen Prototypen, der einen winzigen Ventilator antreibt.
Mit zusätzlicher Spannung kann auch Wasserstoff erzeugt werden, weshalb an eine Kopplung beider Systeme gedacht wird, um die Leistung, die von diesen jeweils produziert wird, zu potenzieren und zu nutzen. Da diese Zellen keine teuren Edelmetalle wie Platin benötigen, rechnet man damit, sie kosteneffizient betreiben zu können. Letztlich sollen sie genügend Strom erzeugen, um eine Kläranlage zu betreiben und dazu noch eine benachbarte Gemeinde zu versorgen. Marktreif könnten die mikrobiellen Brennstoffzellen in 5 – 10 Jahren sein.
In einer Präsentation vom Januar 2013 faßt Logan die zwischenzeitlich gemachten Fortschritte zusammen. Die Fähigkeit bestimmter Mikroorganismen, Elektronen aus der Zelle hinaus zu übertragen, bietet nicht nur die Chance für neue Energieerzeugungsarten wie hier beschriebenen mikrobiellen Brennstoffzellen (MFCs), um elektrische Energie zu erzeugen, bzw. mikrobielle Elektrolysezellen (MEC), um Kraftstoffe wie Wasserstoff und Methan zu produzieren, sondern auch mikrobielle Entsalzungszellen (MDC), die das Wasser teilweise oder vollständig entsalzen, sowie mikrobielle Umkehrelektrodialyse-Zellen (MRCs), die zusätzlich verwendet werden können, um aus dem Salzgehaltsgradienten Energie zu gewinnen.
Es wird sicherlich interessant sein zu verfolgen, ob es dem Team gelingt, aus den einzelnen Elementen ein integriertes, möglicherweise sogar synergetisches System zu schaffen, das sich auch hochskalieren läßt.
Im September 2011 veröffentlichen Prof. László Kálmán
und seine Arbeitsgruppe an der kanadischen Concordia University in
Montreal einen Bericht mit der Aussage, daß sie praktisch umsetzbaren Bio-Batterien einen
großen Schritt näher gekommen sind, indem es ihnen gelungen ist, die
Speicherzeit der elektrischen Ladung einer Enzym-Batterie von Sekunden
auf Stunden zu verlängern. Die Forschung wird durch einen Zuschuß des
kanadischen Natural Sciences and Engineering Research Council finanziert.
Das vorgegebene Ziel war, daß die in der Zellwand eines Bakteriums aus Sonnenlicht, Wasser und CO2 produzierte Energie nicht sofort in Prozessen der Zelle selbst verbraucht, sondern statt dessen gespeichert wird. Dies gelingt dem Team durch die Zugabe verschiedener anderer Moleküle, mit denen der Speicherprozeß immer länger ausgedehnt werden kann.
Für die Erfassung der Sonnenenergie ist das Enzym entscheidend, da das Licht im Enzym eine Ladungstrennung induziert, was bei diesem zu einem negativ geladenen und einem positiv geladenen Ende führt, ähnlich wie in einer Batterie. Indem die Form des Enzyms verändert wird, wird die Energie der Zelle nicht sofort verbraucht sondern kann gespeichert und später abgerufen werden.
In seiner natürlichen Konfiguration ist das Enzym vollkommen in der äußeren Schicht der Zelle eingebettet, die als Lipidmembran bekannt ist, und seine Struktur ermöglicht es, die Ladungen schnell zu rekombinieren und sich von dem ladungsgetrennten Zustand zu erholen. Bilden jedoch verschiedene Lipidmoleküle die Membran, wie bei den Versuchen, kommt es zu einer Fehlanpassung zwischen der Form der Membran und der Form des in sie eingebetteten Enzyms. Sowohl das Enzym als auch die Membran verändern am Ende ihre Form, um eine gute Paßform zu finden. Diese Veränderungen machen es schwieriger für das Enzym, die Ladungen zu rekombinieren, wodurch das elektrische Potential viel länger erhalten bleibt.
Im Februar 2012 melden Wissenschaftler um Prof. Grant
Burgess an der University of Newcastle in Großbritannien,
daß sie mit Hilfe stratosphärischer Bakterien die
Menge der Stromerzeugung in MFCs verdoppeln können. Sie konzentrieren
sich dabei insbesondere auf zwei Arten von Mikroben, Bacillus stratosphericus und Bacillus
altitudinis, die in der Stratosphäre, etwa 45 km über der Erde,
zahlreich auftreten und sich als gute elektrische Leiter erwiesen haben.
Dank des atmosphärischen Kreislauf-Prozesses der Erde kann das Team
die Bakterien aus dem Fluß Wear sammeln und isolieren.
Insgesamt wird die Stromerzeugung von über 75 verschiedenen Arten von Bakterien getestet, indem die Elektroden einer mikrobiellen Brennstoffzelle mit einem speziellen Biofilm beschichtet wird. Sobald dieser ,gefüttert’ wird, produzierten die Bakterien Elektronen, die in die Elektroden geleitet Strom erzeugen. Mit den Stratosphären-Bakterien gelingt es dem Team einen künstlichen Biofilm zu schaffen, der die elektrische Leistung der MFC von 105 W/m3 auf 200 W/m3 fast verdoppelt.
Im November 2012 veröffentlicht Prof. Ozgur Sahin
von der Columbia University in New York seine Erkenntnisse
darüber, daß die Verdunstung die
größte Energiequelle der Natur ist, da ja das gesamte Klima durch Verdampfen
von Wasser aus den Ozeanen angetrieben wird. Allerdings sei ihm bislang
keine Möglichkeit bekannt, Zugriff auf diese Energie zu bekommen. (Anm.:
Meiner Meinung funktioniert das Synergetische Modell – siehe Teil
D – nach eben diesen Prinzipien).
Mit Hilfe von einfachen Lego-Bausteinen gelingt Sahin und seinem Team, die dabei mit Kollegen von der Harvard University und der Loyola University zusammenarbeiten, die Entwicklung eines Bio-Generators, der die Energie des Verdunstungsprozesses auffangen und in Elektrizität umsetzen kann. Die Grundlage dessen ist die Bakterie Bacillus, ein Mikroorganismus, der im Erdboden reichlich vorhanden ist. Sobald diese ,hungert’ , formt sie sich zu einer starren Spore, um zu überleben und ihr genetisches Material zu schützen. Bei höherer Luftfeuchtigkeit absorbiert die Spore wieder Feuchtigkeit aus der Luft und vergrößert ihr Volumen dabei um 40 %, während sich dieser Prozeß unter trockenen Umgebungsbedingungen wiederum umkehrt.
Da eine derartige Größenveränderung bei einem Material, das so starr ist wie Holz oder Kunststoff, sehr ungewöhnlich ist, kommen die Wissenschaftler zu dem Schluß, daß sich erweiternde und schrumpfende Sporen wie ein Muskel funktionieren und zum Beispiel andere Objekten schieben und ziehen können. Zudem erkennen sie, daß sich die Bewegungen der Sporen ernten und in elektrische Energie umwandeln lassen. Immerhin produzieren diese Sporen eine weitaus größere Kraft als die Muskeln eines Menschen (etwa das 1.000-fache), wobei selbst geringe Mengen an Feuchtigkeit bereits eine Bewegung auslösen, die sich ,ernten’ läßt.
Das Team baut daraufhin u.a. aus Lego-Bausteinen einen Prototypengenerator, der einer Windturbine nachempfunden ist und den Nachweis erbringt, daß die Bewegungen der Sporen tatsächlich geerntet werden können. Dafür wird ein elastisches und flexibles Gummiblatt mit einer dünnen Lage aus Sporen beschichtet und mit einem kleinen Generator verbunden. Mithilfe eines Ventilators und einer Schale Wasser, d.h. der trockenen Luft im Labor bzw. der Feuchtigkeit von der Oberfläche des Wassers, kann das gesamte Gummiblatt dazu veranlaßt werden, sich zu wellen und wieder zu strecken. Dadurch rotiert die Turbine vor und zurück und produziert Elektrizität.
Die weitere Forschung, die zu der Entwicklung einer Batterie führen könnte, welche die Energie der Sporen verwenden kann, wird nun vom US-Department of Energy unterstützt, wo man besonderes Interesse daran hat, die Sporen in größere Strukturen einzubauen. Sahin sieht eine mögliche Anwendung in Form einer industriellen Beschichtung aus Sporen, die auf ein flexibles, gummiartiges Material gestrichen werden kann, das sich in Reaktion auf die Luftfeuchtigkeit verdreht. Der potentielle Ertrag soll dem der Solarenergie entsprechen.
Im Juni 2013 stellt ein Forschungsteam der University
of Maryland, das von der National Science Foundation und dem
NanoCenter der Universität unterstützt wird, eine neue wiederaufladbare
Batterie vor, die aus dünnen, mit Zinn ummantelten Holzfasern besteht
und Natriumlösung als Elektrolyt enthält.

Die Nachwuchswissenschaftler Nicholas Weadock, Teng Li und Liangbing Hu entscheiden sich für Holzfasern der Gelbkiefer, welche sowohl flexibel als auch wiederstandsfähig sind. Sie sind 1.000 Mal dünner als ein Blatt Papier und werden zu dünnen Plättchen verwoben. Danach werden sie mit einer dünnen Schicht Zinn ummantelt, die den Stromfluß ermöglicht. Im Gegensatz zu herkömmlichen Batterien wird zudem das Lithium durch Natrium ersetzt.
Eine erste Holzbatterie hat in Test bereits mehr als 400 Ladezyklen überstanden. Nach den Testzyklen sind die Fasern zwar faltig, aber noch immer intakt. Mittels Computermodellen kann abgeleitet werden, daß diese Falten den Streß in der Batterie während des Lade/Entladevorgangs aufnehmen können, was ihnen länger zu überleben hilft. Die Fasern, die weich genug sind, um die Belastung der Veränderungen im Zinn abzupuffern, wenn dieser von Natriumionen durchflossen wird, dienen dabei als Schlüssel zum Erfolg der Batterie.
Der wesentliche Vorteil der Holzbatterie ist jedoch, daß die Kombination von Holz und Natrium äußerst kosteneffizient und umweltfreundlich ist. Dabei liegt die Idee nahe, denn Holzfasern, in denen ein Baum einst mineralreiches Wasser hielt, sind ideal für die Speicherung flüssiger Elektrolyte, so daß sie nicht nur die Basis, sondern sogar einen aktiven Teil der Batterie bilden können.
Ein weiterer mikrobieller Akku, der auf natürlich vorkommenden Bakterien basiert, welche organische Abfälle in Biotreibstoff und Elektrizität umwandeln, wird im September 2013 von einem interdisziplinären Team an der Stanford University um Xing Xie präsentiert.

der Stanford University
Der Prototyp der Forscher besteht aus einem einfachen Glas mit Abwasser, in dem eine negativ und eine positiv geladene Elektrode stecken. Die sogenannten exoelektrogenischen Bakterien kletten sich an die negativ geladene Anode und geben während ihrer Nahrungsaufnahme Elektrizität ab, die von der positiv geladenen Kathode eingefangen wird. Dabei ermutigen Kohlenstoff-Filamente an der negativen Anode die Mikroben dazu, Wein-ähnliche Ranken wachsen zu lassen.
Die Kohlenstoff-Fasern nehmen die von den Mikroben ausgeschiedenen Elektronen auf und führen sie recht effizient zu einer positiven Silber-Anode, wo das Silberoxid zu Silber umgewandelt wird und dadurch die elektrische Energieabgabe der Mikroben effektiv gespeichert wird.
Die Mikroben wandeln (je nach Meßmethode) 44 - 49 % der organischen Masse um, doch die Rückgewinnung der Energie aus dem Silber in festem Zustand läßt den Gesamtwirkungsgrad des Prozesses auf etwa 30% der im Abwasser gespeicherten Energie sinken. Bis zu einem Großeinsatz stehen allerdings weiterführende Experimente und Verfeinerungen an, um den Prozeß durch die Weiterentwicklung und die Suche nach billigeren Materialien kostengünstiger zu machen. So besteht beispielsweise die Kathode des Prototyps derzeit noch aus Silberoxid. Die Verwendung von Silber im großen Stil wäre allerdings kaum wirtschaftlich.
Daß nun auch Tintenfische als neuartige biologische
Quellen für Batterie-Materialien herhalten können, berichten im Dezember 2013 die
Professoren Chris Bettinger und Jay Whitacre von der Carnegie
Mellon University (CMU). Die Wissenschaftler entwickeln eine
biologisch abbaubare Batterie, die sogenannte ,elektronische Pillen’
(smart pills) mit Strom versorgen soll.
Ihr Prototyp verwendet als Anodenmaterial das Pigment Melanin, das der Tinte von Sepien (Echte Tintenfische) – ebenso wie menschlicher Haut sowie Haaren – ihre schwarze Färbung verleiht, während als Kathodenmaterial Manganoxid dient. Beide Stoffe können vom Körper in nicht-toxische Reststoffe abgebaut werden, wenn die Batterie ihre geplante Lebensdauer überschritten hat.
Die Melanin-Batterien erreichen zwar nicht die Leistung von Lithium-Ionen-Batterien, produzieren aber genug Strom, um einfache Sensoren mit Energie zu versorgen. Um die Leistungsfähigkeit der Batterien weiter zu erhöhen, experimentiert Bettingers Gruppe nun mit verschiedenen Melaninvarianten.
Auch andere Forschungsgruppen und Elektronikhersteller arbeiten an elektronischen Pillen. Die Firma Proteus Digital Health aus Palo Alto beispielsweise stellt Pillen her, an denen ein kleiner Chip befestigt ist, der zwischen zwei Metallfolien steckt, die zur Batterie werden, wenn sie mit Ionen in der Magenflüssigkeit in Berührung kommen. Prof. John A. Rogers von der University of Illinois in Urbana-Champaign (der sich ansonsten mit Solarzellen beschäftigt) hat wiederum eine abbaubare Batterie entwickelt, die aus löslichen Metallen und Spurenelementen wie Magnesium und Molybdän besteht.
Im Januar 2014 wird gemeldet, daß ein Forscherteam
der Virginia Tech unter der Leitung von Prof. Y. H. Percival Zhang
eine neue, mit Zucker betriebene Bio-Batterie hergestellt
habe, die eine bislang unübertroffene Energiedichte besitzt. Der Akku,
der auch als enzymatische Brennstoffzelle bezeichnet wird, basiert
auf nicht-immobilisierten Enzymen, die mit einer maximalen Ausgangsleistung
von 0,8 mW/cm2 und
einer maximalen Stromdichte von 6 mA/cm2 weit
höhere Werte aufweisen als Systeme auf Basis immobilisierter Enzyme.
Zhang und seine Kollegen konstruieren hierfür einen nicht-natürlichen, synthetischen enzymatischen Weg, der alle Ladungspotentiale aus dem Zucker zur Stromerzeugung abzieht, wobei als Katalysator anstelle von Platin günstige Biokatalysator-Enzyme verwendet werden. Das Ergebnis kann sich sehen lassen: Der Zucker-Batterie kombiniert Maltodextrin (ein Polysaccharid, das aus der teilweisen Hydrolyse von Stärke gewonnen wird) mit Luft, um als ,Hauptnebenprodukte’ Strom und Wasser zu erwirtschaften. Dabei erreichen enzymatische Brennstoffzellen, die eine 15 %-ige Maltodextrin-Lösung enthalten, eine Energie-Speicherdichte von 596 Ah/kg, was um eine Größenordnung höher ist als die von Li-Io-Batterien.
Die Kraftstoff-Zuckerlösung ist weder explosiv noch brennbar, dafür aber biologisch abbaubar. Außerdem ist die Batterie nachfüllbar, denn Zucker kann so ähnlich hinzugefügt werden, wie das Auffüllen einer Druckerpatrone mit Tinte. Die Wissenschaftler hoffen, die Marktreife in drei Jahren erreichen zu können. Unterstützung für die aktuelle Forschung kommt von der Virginia Tech und der Firma Cell-Free Bioinnovations Inc., die hierfür eine zusätzliche Finanzierung durch einen Small Business Innovation Research grant der National Science Foundation erhält.
Eine
Wasserbatterie betreibt auch die Wanduhr der Firma Bedol, die im März 2014 für
89 $ auf den Markt kommt. Kleinere Tischuhren und Wecker gibt es schon
ab 26 $.
Weiter mit den verschiedenen Batterie- und Akkumulatorentypen...