Buch der Synergie

| Blättern |
 TEIL C
TEIL C
MICRO ENERGY HARVESTING
MuskulÄre
Systeme (II)
Im August 2007 erscheint ein Bericht
von Sukho
Park, Jinseok Kim und ihren Kollegen an der Chonnam
National University in Südkorea, die
einen krabbenähnlichen Roboter entwickelt haben, der weniger dick
als ein Fingernagel ist und durch die Kontraktionen von Herzgewebe angetrieben
wird, welches seine Energie aus Glukose gewinnt.

Im vorliegenden Fall lassen die Wissenschaftler Herzmuskelgewebe einer Ratte auf einem winzigen Skelett aus Polydimethylsiloxan (PDMS) wachsen, einem biokompatiblen Polymer, das den Roboter geeignet macht zur Verwendung in biomedizinischen Anwendungen. Der Oberfläche des Materials wird in einem speziellen Prozeß ein 3D-Muster aufgeprägt, um das Wachstum der Herzmuskelzellen in die richtige Richtung zu lenken.
Der Roboterkörper verfügt über drei kurze Vorderbeine (400 µm lang) und drei längere Hinterbeine (1.200 µm), die alle an einem zentralen, rechteckigen Quersteg befestigt sind. Sobald sich die Herzzellen (Kardiomyozyten) beim periodischen Schlagen zusammenziehen, biegen sich die längeren Hinterbeine nach innen, was zu einem Unterschied in der Reibung zwischen den vorderen und hinteren Beinen führt und den Roboter mit hoher Zuverlässigkeit und einer Durchschnittsgeschwindigkeit von 100 µm pro Sekunde vorwärts treibt.
Die neuen Mikroroboter können sich über zehn Tage lang kontinuierlich bewegen, wobei sie innerhalb einer Woche eine Strecke von 50 m zurücklegen. In Zukunft sollen sie im Inneren des menschlichen Körpers verwendet werden, um beispielsweise Verstopfungen in Blutgefäßen zu beseitigen, indem sie wie Schiffe dorthin reisen und dann direkt am Ort der Blockade ein Lösemittel freisetzen.
Der Artikel ‚Establishment of a fabrication method for a long-term actuated hybrid cell robot‘ erscheint im Dezember, danach scheint die Angelegenheit aber nicht weiter verfolgt worden zu sein.
Prof. Kevin Kit Parker und
sein Team von der Harvard
University beschreiben in einer Veröffentlichung vom September 2007 die
Herstellung muskulärer Dünnfilme, um damit Aktoren
und ähnliche Geräte zu bauen. Der Bericht trägt
den Titel ‚Muscular thin films for building actuators and powering
devices‘.
Die Plastikfolien, die Kräfte ausüben können, bestehen aus Polydimethylsiloxan, dem eine 3D-Struktur aus mikroskopischen Mustern aufgeprägt wird, die dann mit Herzmuskelzellen von Ratten ,belebt’ wird. Das besondere dabei ist, daß sich die muskulären Dünnfilme in unterschiedliche Formen bringen lassen – etwa als Greifwerkzeuge oder Flossen. Als schwimmende Geschöpfe können sie darüber hinaus von außen mit elektrischen Feldern gesteuert werden, um sich beispielsweise durch eine Petrischale zu bewegen.

Die einzelnen Stücke der zuckenden muskulären Dünnschichten sind nur ein paar Millimeter lang und 30 µm dick. Sie könnten damit als Aktuatoren für winzige Robotervorrichtungen in den Körper implantiert werden, wo die Muskelzellen vom Zucker aus der Blutbahn leben und von den gleichen Reparaturmechanismen gepflegt werden würden, die das Herz am Pumpen halten. Möglicherweise könnte die Muskel-beschichtete Folie auch verwendet werden, um Gewebe zu regenerieren, das bei einem Herzinfarkt beschädigt wurde.
Im Gegensatz zu den bisherigen Ansätzen findet das u.a. von der DARPA finanzierte Harvard-Team Wege, um die Gewebe so leistungsfähig zu machen, daß Kräfte frei werden, die denen des natürlichen Herzgewebes entsprechen: pro Quadratmillimeter bis zu 4 mN. Bisher haben die Forscher nur Rattenzellen verwendet, wollen sich zukünftig aber auch mit menschlichen Zellen befassen.
Im Juli 2012 melden die Fachblogs die Entwicklung einer Robot-Qualle aus Silikon, die von Muskelzellen aus einem Rattenherz angetrieben wird und wie eine Blume mit acht Blütenblättern aussieht. Neben Parker ist daran hauptsächlich der Ingenieur John Oluseun Dabiri vom California Institute of Technology (Caltech) in Pasadena beteiligt, der uns bereits bei den Insekten und Weichtieren begegnet ist und der sich auch mit diversen anderen Energiegewinnungsmethoden beschäftigt, wie z.B. Senkrechtachsern.
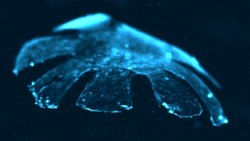
Der nun geschaffene Medusoid, der die Muskelstruktur einer Qualle nachahmt, bildet für die Wissenschaftler eine Möglichkeit, die ,Grundgesetze der muskulären Pumpen’ besser zu verstehen, mit deren Erforschung sich Parker bereits seit 2007 befaßt. Er hatte damals die Doktorandin Janna Nawroth am Caltech damit beauftragt, die Zellen im Körpern junger Ohrenquallen (Aurelia aurita) genau zu kartieren, um zu verstehen wie diese schwimmen.
Der Schirm der Ohrenqualle besteht aus einer einzigen Muskelschicht aus Fasern, die eng ausgerichtet um einen zentralen Ring und entlang acht Speichen verlaufen. Um den Schirm abwärts schlagen zu lassen, laufen elektrische Signale in einer sanften Welle durch den Muskel, was laut Parker so ähnlich aussieht, wie wenn man einen Stein ins Wasser wirft. Er geht deshalb davon aus, daß sich auch bei einer muskulären Pumpe die elektrische Aktivität als Wellenfront zu verbreiten hat.
Im Labor wird eine Struktur mit den gleichen Eigenschaften erzeugt, indem eine einzige Schicht von Ratten-Herzmuskeln auf einer geprägten Folie aus Polydimethylsiloxan kultiviert wird. Wird nun ein elektrisches Feld an die Struktur angelegt, kontrahiert der Muskel schnell, preßt den Medusoiden zusammen und imitiert einen Arbeitstakt der Qualle. Das elastische Silikon zieht den Medusoiden dann wieder in seine ursprüngliche flache Form zurück, bereit für den nächsten Schlag.
Wird die synthetische Kreatur zwischen zwei Elektroden in Salzwasser gelegt, schwimmt sie durch Ausdehnen und Zusammenziehen genauso pulsierend herum wie ihr lebendes Gegenstück. Dabei werden sogar Wasserströmungen erzeugt, ähnlich denen, die Nahrungsteilchen in den Mund der Qualle spülen. Das Team plant nun, einen Medusoiden aus menschlichen Herzzellen zu bauen. Zudem wollen die Forscher versuchen, der Qualle ein einfaches ,Gehirn’ zu geben. Außerdem beantragen sie ein Patent, bei dem ihr Design – oder ein ähnliches – als Plattform für Medikamententests verwendet wird.

(links)
Juli 2016 stellt das Parker-Team einen schwimmfähigen Roboter-Rochen vor, der aus einem Mix aus Kunststoff und lebenden Zellen besteht und nicht nur wie das natürliche Vorbild aussieht, sondern sich mit wellenförmigen Flossenbewegungen auch genauso fortbewegt.
Das künstliche Tier besitzt ein Skelett aus Gold, das mit elastischem Kunststoff überzogen ist. Angetrieben wird es durch etwa 200.000 Herzmuskelzellen von Ratten, die über die gesamte Oberfläche der Kunststoffhaut verteilt sind und die gentechnisch eingebaute Eigenschaft haben, sich auf Lichtsignale hin zusammenzuziehen.
Damit sich der 16 mm lange und nur 10 mg wiegende Cyborg-Rochen gezielt fortbewegt, wird er punktgenau per Lichtsignal gesteuert. Durch die Kontraktion der Muskelzellen schwimmt der Rochen nach unten, während die Aufwärtsbewegung passiv abläuft. Dabei ist das Skelett so konzipiert, daß es einen Teil der Abwärtsenergie zwischenspeichert, um die Flosse dann wieder aufwärts zu bewegen. Es gelingt den Forschern, den künstlichen Rochen so zu steuern, daß er mit einer Geschwindigkeit von 1,5 mm/s einen Parkour bewältigt und Hindernisse umschwimmt, indem die linke und rechte Flosse getrennt mit Lichtsignalen aktiviert werden.
Statt in Wasser kann das hybride Tier allerdings nur in einer Nährstofflösung abtauchen, da diese die Herzmuskelzellen am Leben hält.

Fisch
Gemeinsam mit Forschern der Emory University berichtet das Parker-Team im Februar 2022, daß es zwischenzeitlich einen sich selbständig fortbewegenden bio-hybriden Fisch geschaffen hat, der zum Teil aus menschlichen Stammzell-Herzmuskelzellen besteht. Der Fisch wird vorangetrieben, indem er die Muskelkontraktionen eines pumpenden Herzens nachahmt, und kann monatelang autonom schwimmen, während die Zellen schlagen (‚An autonomously swimming biohybrid fish designed with human cardiac biophysics‘, im Netz einsehbar).
Konstruiert ist der Fisch aus Kunststoff, Gelantine und einer Schwanzflosse, die aus zwei Schichten menschlicher Herzzellen besteht, die aus Stammzellen gewonnenen werden. Er macht sich den Herzautomatismus zunutze, d.h. die mechanisch elektrischen Signale zwischen den beiden Muskelschichten werden dazu genutzt, um Kontraktionen zu erzeugen, auf die jeweils auf der Gegenseite eine Reaktion erfolgt, was zu einer Vortriebsbewegung der Schwanzflosse führt.
Nach Angaben der Forscher schwimmt der Roboterfisch so insgesamt 108 Tage lang in einer Nährlösung, wobei zu beobachteten war, daß der Fisch mit zunehmendem Alter im ersten Monat leistungsfähiger wurde, weil die Herzzellen reiften. Die im gesamten Zeitraum erreichten Flossenbewegungen würden rund 38 Millionen Herzschlägen entsprechen. Das Projekt gilt als ein Zwischenschritt auf dem Weg zur Züchtung kompletter neuer funktionsfähiger Herzen für Transplantationen.
Fast zeitgleich wie oben wird im September 2007 von
einer Gruppe um Yonas
Tadesse an
der University of Texas in Dallas übrigens eine Roboter-Qualle
namens RoboJelly gebaut, die allerdings künstliche
Muskeln aus Nickel-Titanium Memory-Metall besitzt
und durch eine Reaktionen mit Sauerstoff und Wasserstoff angetrieben
wird – und nicht durch Muskelzellen - weshalb sie hier auch nicht weiter
behandelt wird.

(Grafik)
Ebenfalls von Herzzellen angetrieben wird hingegen
der Roboter von Prof. Rashid
Bashir und seinen Kollegen an der University of Illinois
at Urbana-Champaign (UIUC), der im November 2012 in
die Presse kommt.
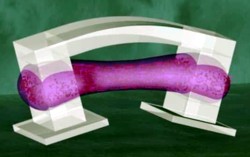
Der etwa 7 mm lange Bio-Bot, der hauptsächlich aus einem flexiblen Hydrogel besteht und mit einem 3D-Drucker hergestellt ist, bewegt sich aufgrund einer Asymmetrie vorwärts. Wie ein kleines Sprungbrett hat der Bot ein langes, dünnes Bein, das auf einem dicken Stützbein ruht. Das dünne Bein ist mit Herzzellen einer Ratte bedeckt, deren Schlagen das Bein dazu veranlaßt, zu schwingen und den Roboter damit vorwärts zu treiben.
Die Fähigkeit, selbständig zu ,gehen’, beschränkt sich gegenwärtig auf eine relativ konstante Geschwindigkeit von 236 µm pro Sekunde bei einer Schlagfrequenz von rund 1,5 Hz. Das Team hofft jedoch schon bald in der Lage zu sein, die Bewegungen des Roboters durch die Zugabe von Neuronen oder von Zellen, die auf Licht reagieren, lenken zu können. Andere Zellen, die auf bestimmte Chemikalien reagieren, könnten dem Bio-Bot zudem Sensor-ähnliche Qualitäen geben.
Außerdem möchten die Forscher ihren halbsynthetischen Kreaturen mehr Funktionalität hinzufügen und suchen bereits nach verschiedenen Formen mit unterschiedlichen Zahlen von Beinen, sowie Roboter, die Steigungen oder Treppen hinauf klettern können.
(Grafik)
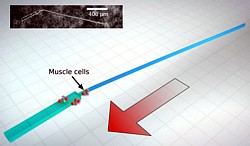
Im Januar 2014 folgt eine weitere Veröffentlichung des UIUC-Teams, die diesmal von Prof. Taher Saif präsentiert wird. Der neue Bio-Bot, der aus Polydimethylsiloxan besteht, besitzt eine synthetische Flagelle, die dem Schwanz eines Spermium ähnelt und von einigen Herzmuskelzellen in Bewegung versetzt wird.
Mit der Flagelle hat der biohybride Schwimmer eine Gesamtlänge von knapp 2 mm und erreicht eine Geschwindigkeit von bis zu 10 µm/s. Eine Variante mit zwei Flagellen schafft sogar rund 80 µ/s. Die Konstruktion mit der Doppelflagelle hat zudem den Vorteil, daß sie sich in Zukunft womöglich in verschiedene Richtungen steuern läßt.
Die Tests der Biobots finden in einer Nährlösung statt, die als Energielieferant für die Zellen dient und unter anderem Salze, eine spezielle Form von Glukose und diverse Vitamine enthält, welche die Herzzellen etwa drei Tage lang am Leben erhalten. Wie sich diese untereinander organisieren und miteinander kommunizieren, um im selben Moment zu kontrahieren, haben die Forscher allerdings noch nicht klären können.
(Grafik)
Schon im Juli zeigt das Team um Prof. Bashir einen Bio-Bot von weniger als 1 cm Länge, der aus 3D-gedrucktem Hydrogel und Rückenmuskel-Gewebe gebaut ist und in Reaktion auf ein elektrisches Signal ,laufen’ kann. Im Gegensatz zu dem in früheren Versionen verwendeten Herzmuskelgewebe, das ständig von selbst kontrahiert und daher nicht kontrollierbar ist, reagiert ein Rückenmuskel auf elektrische Reize, um ihn zur Kontraktion zu führen.
Nachdem der sehr einfach designte erste Bio-Roboter – zwei Füße, eine flexible Wirbelsäule und ein kontrahierender Muskel – die Machbarkeit der Technologie bewiesen hat, wendet sich das Team komplexeren Maschinen zu. Zudem will man versuchen, Neuronen zu integrieren, um den Bot in verschiedene Richtungen laufen lassen zu können, wenn er mit verschiedenen Reizen konfrontiert wird, wie z.B. Licht oder chemische Gradienten als Auslöser.

Rückenmuskel-Bio-Bot
Im März 2016 wird bestätigt, daß die Lichtsteuerung des Bio-Bots inzwischen verwirklicht werden konnte. Die jeweils 7 mm bis 2 cm langen Vorrichtungen, bei denen die 3D-gedruckten Füße von einem Ring aus Muskelgewebe umschlungen werden, welches aus Mäuse-Zellen gezüchtet ist, kontrahieren, sobald sie einer bestimmten Wellenlänge von blauem Licht ausgesetzt werden. Nach ihrer Herstellung werden die Muskelringe mit regelmäßigen Impulsen dieses Lichtes bestrahlt, um durch dieses ,Training’ größer und stärker zu werden.
Im Gegensatz zu dem Ansatz, die Muskeln durch elektrische Stimulation zu steuern, wobei der ganze Muskelring auf einmal kontrahiert, hat Licht mehrere Vorteile. Zum einen können elektrische Ströme biologisches Gewebe beschädigen, während das blaue Licht harmlos ist. Zum anderen kann das Licht auf bestimmte Teile des Bio-Bots fokussiert werden, sodaß nur dieser Bereich kontrahiert, was eine feinere Lenkungskontrolle ermöglicht und auch verwendet werden könnte, die Bots in Richtung einer Lichtquelle zu führen. Denkbar sind damit auch komplexere Skelette mit mehreren Muskelringen, von denen jeder für die Bewegen eines bestimmten Fortsatzes verantwortlich ist.
Die Arbeiten sind Teil des Projekts ,Emergent Behaviors of Integrated Cellular Systems’ (EBICS), das von der National Science Foundation (NSF) finanziert wird und bereits im Herbst 2015 eine weitere Fünf-Jahres-Förderung in Höhe von 25 Mio. $ erhielt, um eine Vielzahl von Anwendungen in der Diagnostik, Medizin und Sensorik zu entwickeln.
Im Februar 2017 veröffentlicht das Forscherteam von Prof. Bashir eine Anleitung zum Bau von Muskelzellen-betriebenen Bio-Bots (‚A modular approach to the design, fabrication, and characterization of muscle-powered biological machines‘). Die wissenschaftliche Arbeit beinhaltet nicht nur die schrittweise Anleitung – vom 3D-Druck des Gerüsts bis hin zum Tissue Engineering – sondern auch eine Liste der benötigten Geräte und Hilfsmittel für den Prozeß. Dies soll Wissenschaftlern weltweit ermöglichen, selbst Bio-Bots für eine Reihe von Anwendungen zu kreieren.
(Grafik)
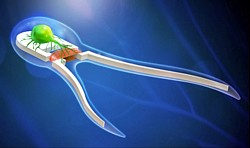
Über das Team von Prof. Saif ist im September 2019 wieder etwas zu erfahren, als es im Zuge einer Veröffentlichung unter dem Titel ‚Neuromuscular actuation of biohybrid motile bots‘ über die jüngsten Entwicklungen berichtet. Dabei handelt es sich um biohybride Roboter, die allein durch eine Mischung aus motorischen Neuronen, integrierten schlagenden Herzzellen und Licht angetrieben werden.
Die winzigen, weichen Bio-Bots, die aus eigener Kraft in biologischen Umgebungen wie dem menschlichen Körper laufen und schwimmen können können, sind Spermien nachempfunden. Die erste Generation mit einem Schwanz nutzt zwar Herzgewebe, das von sich aus schlägt, kann aber weder die Umgebung wahrnehmen noch Entscheidungen treffen.
Um die Konstruktion weiter zu verbessern, entwickelt das Team ein neues Design, das zwei Schwänze anstelle von einem hat. Es besteht aus einem weichen Gerüst, das mit Skelettmuskelgewebe und lichtempfindlichen Motoneuronen aus Mäusestammzellen beschichtet ist. Bei Lichteinfall feuern die Neuronen und werden zu Aktuatoren, die das Muskelgewebe in Gang setzen und den Roboter vorwärts treiben.
Eine weitere Meldung stammt vom April 2020 und besagt, daß die obigen Bio-Bots zwischenzeitlich durch ein Team unter der Leitung von Prof. Martha Gillette ein Upgrade in Form von Rückenmarksgewebe erhalten haben, das sie im Wesentlichen selbständig macht (‚Emergence of functional neuromuscular junctions in an engineered, multicellular spinal cord-muscle bioactuator‘).
Zr Umsetzung wird einer Ratte entnommenes Lendenwirbelgewebe in einen Bio-Bot-Körper eingesetzt und dann sieben Tage lang zusammen mit dem Rückenmuskelgewebe kultiviert, so daß sich Verbindungen zwischen beiden bilden. Gewebe aus der Lendengegend zu verwenden, ist deshalb wichtig, weil es den ‚Schaltkreis‘ enthält, der den Links-Rechts-Wechsel der Beine beim Gehen steuert.
Wird nun Glutamat als Neurotransmitter hinzugefügt, veranlaßt dieses das Rückenmarkgewebe, Signale an das Muskelgewebe zu senden, wodurch sich letzteres wiederholt und kontinuierlich zusammenzieht und den Roboter dazu bringt, sich in einem ‚natürlichen Gehrhythmus vorwärts zu bewegen. Sobald jedoch ein Glutamat-Inhibitor hinzugefügt wird, hört das Laufen auf.
In einem Bericht vom November 2008 wird die Idee
des Elektrophysiologen Paul Roberts am University
Hospital Southampton (UHS) in Großbritannien beschrieben,
die für einen Herzschrittmacher benötigte Energie mittels eines durch
den Blutdruck hin und her bewegten Magneten zu gewinnen.
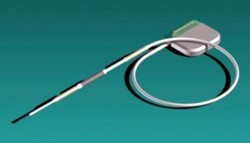
Der Generator besteht aus zwei kleinen, flüssigkeitsgefüllten Ballons, die an getrennten Orten innerhalb des Herzens positioniert und durch einen Silikonschlauch verbunden sind, der einen beweglichen Magneten enthält. Wenn das Herz schlägt, quetscht es abwechselnd jeden der Ballons, drückt dabei die Flüssigkeit durch das Rohr und zwingt damit den Magneten, sich an einer in das Rohr eingebetteten Spule vorbei hin und her zu bewegen und Elektrizität zu erzeugen.
Bislang ist das System aber noch nicht in der Lage, ausreichend Energie für einen Herzschrittmacher bereitzustellen. Ein Prototyp, der in einem Schwein getestet wird, produziert mit 4,3 mJ pro Herzschlag nur 17 % der Energie, die eigentlich dafür benötigt wird.
(Grafik)
Roberts behauptet, daß Verbesserungen an dem Polymer, der für die Ballons verwendet wird, die Effizienz zukünftiger Modelle mehr als verdoppeln könnte. Für die Weiterentwicklung bemüht er sich um staatliche Mittel – und sucht auch schon potentielle Geschäftspartner, um den neuen Generator zu kommerzialisieren.
Im März 2009 werden dann einige weitere Details bekannt. Dem zufolge wurde das Projekt, das einen Mikrogenerator namens ,Self-Energizing Implantable Medical Microsystem’ (SIMM) in den vergangenen zwei Jahren in Zusammenarbeit mit einem Unternehmenskonsortium entwickelt hat, Ende 2006 mit gut 520.000 £ vom Technology Strategy Board der britischen Regierung unterstützt. Neben verschiedenen Ärzten, einschließlich Roberts, sind die Firmen Perpetuum, Zarlink Semiconductor und InVivo Technology beteiligt. Weiterführende Schritte ließen sich bisher aber nicht dokumentieren.
Auch über Geräte, die vom Herzschlag des ganzen Organs
gespeist werden, gibt es einiges zu berichten.
Im Februar 2009 melden die Fachblogs, daß eine Forschungsgruppe am Georgia Institute of Technology (Georgia Tech) um Prof. Zhong Lin Wang einem Hamster eine Jacke mit Nanogeneratoren angezogen habe, mit der das Tier Strom erzeugt, sobald es in seinem Laufrad losrennt. Mit der gleichen Nanotechnologie gelingt es aber auch, elektrischen Strom durch tippende Finger zu gewinnen, so daß sich Geräte wie Mobiltelefone und PDAs eines Tages durch das Tippen von SMS oder Texten aufladen lassen könnten – worauf ich etwas weiter unten noch ausführlich zu sprechen komme. Auch die Entwicklung der piezoelektrischen Zinkoxid-Nanodrähte, auf denen diese Nanogeneratoren aufbauen, beschreibe noch detailliert (s.d.).

Über medizinische Geräte, welche vom Herzschlag des Patienten gespeist werden, ist im Juni 2010 zu erfahren. Bei den Versuchen gelingt es dem Team des Georgia Tech, mit einem kleinen, fast unsichtbaren Nanodraht die Energie der pulsierenden, sich biegenden Muskeln innerhalb eines Rattenkörpers in elektrischen Strom umzuwandeln.
Hierzu wird ein entsprechender Nanodraht auf ein flexibles Polymersubstrat aufgebracht und die Vorrichtung anschließend mit einem Polymer ummantelt, um sie vor Körperflüssigkeiten zu schützen. Wird der 2 x 5 mm große Wandler an dem Zwerchfell der Ratte befestigt, streckt die Atmung des Nagetiers den Nanodraht, wobei vier Picoampere (pA) Strom bei 2 mV erzeugt werden. Direkt am Rattenherz angebracht, können sogar 30 pA bei 3 mV erreicht werden.
Solche Zinkoxid-Nanogeneratoren wären ideal für Geräte innerhalb des Körpers, die beispielsweise den Blutdruck oder den Blutzuckerspiegel messen. Die Herausforderung ist nun herauszufinden, wie das Material dazu gebracht werden kann eine ausreichend hohe Leistung zu erzielen, um solche Geräte zu betreiben. Da die kinetische Energie innerhalb des Körpers nur in kleinen Dosen auftritt, untersuchen die Forscher auch, wie aus den verfügbaren Quellen so viel Energie wie möglich gesammelt werden kann, um die Vorrichtungen lange am Laufen zu halten.
Im August 2011 kündigt der kolumbianische Elektro-
und Bioingenieur Jorge Reynolds Pombo, Erfinder des
ersten externen Herzschrittmachers mit Innenelektroden, der
von einer 12 V Batterie gespeist wurde (1958),
die Einführung eines neuartigen Schrittmachers an,
der so klein wie ein Drittel Reiskorn ist und keine Batterie benötigt.
Leider ist es mir bislang nicht gelungen, nähere Details oder Informationen
über diese Innovation zu finden.
Der Praktiker beschäftigt sich seit 1991 übrigens auch damit, die Herzen der Wale zu studieren, die denen der Menschen ähnlich sein sollen, wofür er mit U-Booten der Marine von Kolumbien sechs akustische Unterwasserforschungsfahrten durchführt.
Im Februar 2012 berichtet die Presse, daß Forscher
der University of Michigan daran arbeiten, piezoelektrische
Materialien bei Herzschrittmachern anwenden, um mit den vom schlagenden
Herzen ausgelösten Vibrationen die Energie zu erzeugen, die
der Herzschrittmacher für seinen Betrieb benötigt. Damit wären die
bislang alle 7 – 10 Jahre erforderlichen Operationen zum Austausch
der Batterien überflüssig, was nicht nur die Patienten entlasten, sondern
auch dem öffentlichen Gesundheitssystem beträchtliche Kosten ersparen
würde.
Immerhin bildet Herzinsuffizienz heute in Europa und den Vereinigten Staaten einen der größten Kostenmacher. Weltweit haben zu diesem Zeitpunkt mehr als drei Millionen Menschen Herzschrittmacher, während jedes Jahr über 1.000.000 Geräte neu implantiert werden. Ein weiterer Vorteil der batterielosen Schrittmacher ist, daß sie nicht durch die Magnetfelder von Analysegeräten wie z.B. der Magnetresonanztomographie betroffen sind.
Das Team um den Luftfahrttechnik-Experten M. Amin Karami, der sich bislang damit beschäftigt hatte, bei unbemannten Flugzeugen mittels Spezialkeramiken Strom aus den Schwingungen der Flügel gewinnen (s.u. Vibration), baut noch keinen Prototypen, sondern untersucht zunächst mit Simulationen, ob lineare und nichtlineare piezoelektrische Vorrichtungen überhaupt eine ausreichende Energiemenge liefern können. Hierfür wird ein virtuelles Modell konstruiert, dessen Keramikschicht präzise in eine Form gebracht ist, die Schwingungen in einem breiten Frequenzbereich ernten kann. Zudem werden Magnete eingearbeitet, deren zusätzliches Kraftfeld das elektrische Signal drastisch steigern können, weches aus den Schwingungen resultiert.

Die Wissenschaftler kommen zu dem Schluß, daß eine Piezokeramik mit einem Ausmaß von maximal 27 x 27 x 6 mm eine Leistung von 10 µW erreichen sollte, was etwa der achtfachen Menge entspricht, die ein Schrittmacher benötigt. Damit könne ein Schrittmacher im Bereich von 7 – 700 Schlägen pro Minute betrieben werden (spätere Aussage: 20 – 600 Schläge). Die Arbeiten erhalten Unterstützung vom National Institute of Standards and Technology (NIST) und dem Institute for Critical Technology and Applied Science (ICTAS) der Virginia Polytechnic Institute and State University (Virginia Tech).
Im November 2012 folgt die Meldung, daß das Team zwischenzeitlich auch eine Versuchsanordnung entwickelt habe, in der die kraftvolle Vibration, welche der Herzschlag im Körper erzeugt, mit Magneten erfaßt und gespeichert wird. Bei Tests ist die Vorrichtung in der Lage, die 10-fache Energiemenge zu liefern, die ein Schrittmacher benötigt.
Daniel J. Inman, Karamis wichtigster Kollege und Vorsitzender der universitären Entwicklungsabteilung für Luft- und Raumfahrt, berichtet Anfang 2013, daß man nun auch bewiesen habe, daß ein 0,25 mm langes Stück des piezoelektrischen Materials 18 µW Leistung erzeugen kann, was ausreicht um 18 Herzschrittmacher zu betreiben. Das nächste Ziel des Teams besteht nun darin, einen kleineren, stabilen und voll funktionsfähigen herzbetriebenen Schrittmacher zu entwickeln.
Karami wird 2013 Professor an der University of Buffalo, umd im Mai 2015 veröffentlichen Karami und Inman einen Bericht über ihre Arbeiten mit dem Titel ‚Powering Pacemakers with Heartbeat Vibrations‘ – danach ist aber nichts mehr darüber zu hören.
Meldungen im Mai 2011 zufolge forscht das Heart-Beat
Scavenger Consortium (HBS) in Frankreich ebenfalls daran,
piezomagnetische Materialien zur Stromversorgung von Herzschrittmachern
zu verwenden. Die Experten des Konsortiums, das neben dem CEA-Leti
die Sorin Group, TIMA, Cedrat Technologies, Tronics und EASII IC umfaßt,
wollen durch das Bündeln ihres Know-how einen energieautarken Herzschrittmacher
entwickeln, der mit nur einen Kubikzentimeter etwa achtmal kleiner
ist als die aktuellen Modelle. Ein längerfristiges Ziel des Projekts
ist e,s die Gesundheitsausgaben zu senken.
Das Leti (Laboratoire d’electronique des technologies de l’information) ist ein großes Forschungsinstitut für Elektronik und Informationstechnologie mit Sitz in Grenoble, das 1967 als Tochtergesellschaft des staatlichen Kommissariats für Atomenergie und alternative Energien (Commissariat à l’énergie atomique et aux énergies alternatives, CEA) gegründet wurde.
Finanziert wird das HBS durch das seit 2005 bestehende, ebenfalls staatliche Minalogic Kompetenzzentrum in Grenoble. Deshalb ist es eigentlich überraschend, daß man danach nichts Neues mehr von dieser Initiative vernimmt.
Einen ganz anderen Ansatz verfolgen Wissenschaftler des Artificial
Organ Center for Biomedical Engineering Research (Artorg) der Universität
Bern, wie im Juli 2011 zu erfahren ist.
Ein Team um den Schweizer Kardiologen Prof. Rolf Vogel und
seinen Mitarbeiter und Doktoranden Adrian Zurbuchen arbeitet
seit 2008 an verschiedenen Techniken, die einen
Herzschrittmacher über das Schlagen des patienteneigenen Herzens mit Energie versorgen sollen, worunter sich – sehr schweizerisch
– auch ein von einer Armbanduhr inspiriertes Gerät befindet.

Der im September 2014 vorgestellte Prototyp ist aber nicht nur durch eine Armbanduhr inspiriert, sondern beinhaltet tatsächlich den Autoaufzug-Mechanismus eines handelsüblichen Modells. Dieser nutzt die Armbewegungen des Trägers, um eine winzige mechanische, spiralförmige Feder aufzuwickeln. Sobald diese vollständig aufgezogen ist, entspannt sie sich wieder und betreibt dabei einen Mikrogenerator im Inneren der Uhr.
Im Fall des Berner Geräts soll das miniaturisierte Aufzieh-Uhrwerk an die pulsierende Außenwand des menschlichen Herzens genäht, anstatt am Handgelenk getragen zu werden, und die Feder wird von Herzkontraktionen statt von Armbewegungen aufgewickelt. Die vom Abwickeln resultierende Energie wird dann in einem Kondensator gepuffert, welcher wiederum den Herzschrittmacher betreibt, mit dem er elektrisch verdrahtet ist. Als das System einem lebenden, 60 kg schweren Schwein implantiert wird, zeigt es eine mittlere Ausgangsleistung von 52 µW, was mehr als genug ist für die meisten modernen Herzschrittmacher, die 5 - 10 µW verbrauchen.
In einem Pressebericht vom März 2017 werden noch einige Details über den Uhrwerk-Prototypen genannt, der direkt auf das Schweineherz genäht wurde. Dieser wiegt etwa 12 g, also weniger als die Hälfte eines üblichen Herzschrittmachers. Das gesamte Uhrwerk-System nimmt dabei rund 7,7 g ein. Das äußere Gehäuse hat einen Durchmesser von rund 2,7 cm und eine Dicke von nicht einmal 1 cm. Ein batteriebetriebener Schrittmacher ist ungefähr doppelt so groß.
Als nächstes soll die Technologie weiter miniaturisiert und empfindlicher für die Bewegung des Herzens gemacht werden. Zudem will man versuchen, sowohl die Energie-Ernte-, als auch die Kondensator-Funktion innerhalb eines Herzschrittmachers einbauen. An der Finanzierung des Projekts beteiligt sich auch das Schweizer Bundesamt für Forschung.
In der Meldung von 2011 werden übrigens noch zwei weitere Techniken erwähnt, die von den Forschern untersucht werden, einmal eine Art ,Flußkraftwerk’, und zum anderen ein ,Arterien-Mantel’. Bei dem ersten Ansatz geht es im Prinzip darum, die bereits bestehende Flußkraftwerk-Technologie so zu verkleinern, daß eine Turbine in eine Arterie in Herznähe paßt. Bewegliche Teile, die sich im Blutkreislauf befinden, bedeuten ein besonderes Risiko. Mehr darüber berichte ich unter Strömung (s.d.).
(Grafik)
Der Arterien-Mantel wiederum nutzt den Effekt der sogenannten Magnetohydrodynamik und die Elastizität der Blutgefäße, wobei ein dehnbarer Kunststoff-Mantel um eine Arterie gelegt wird. Innerhalb des Mantels befindet sich eine stark leitfähige Flüssigkeit, welche durch die Kontraktion und die Ausdehnung der Arterie, wenn das Herz Blut durchpumpt, in Bewegung gerät. Dadurch wird ein schwaches elektromagnetisches Feld erzeugt, welches als Stromquelle angezapft werden kann, wobei die Energieausbeute allerdings relativ gering ist. Ob inzwischen tatsächlich, wie geplant, der Prototyp eines Mantels hergestellt worden ist, konnte ich jedoch nicht herausfinden.
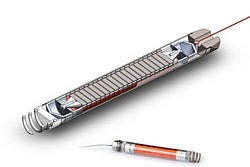
Die im November 2017 veröffentlichte Studie ‚Endocardial Energy Harvesting by Electromagnetic Induction‘ befaßt sich mit einer weiteren Version, einem kleinen Minigenerator aus Magneten und Spulen, der mit einem Katheter in die rechte Seite des Herzens implantieren werden könnte, wo er mit jedem Muskelschlag bewegt wird und die endokardialen Herzbewegungen in elektrische Energie für den Schrittmacher umwandelt.
Während eines Tierversuchs erntet das implantierte Gerät eine mittlere Ausgangsleistung von 0,78 μW und 1,7 μW bei einer Herzfrequenz von 84 bzw. 160 Schlägen pro Minute. Ein mathematische Modell prognostiziert sogar Leistungen zwischen 14,5 μW und 16,9 μW. Wegen der Magnete im Harvester müßte ein damit ausgestatteter Patient allerdings auf MRI-Untersuchungen verzichten.
Herzschrittmacher
An der Université Paris-Sud stellt Martin
Deterre im Juli 2013 im Rahmes seiner Dissertation
eine Arbeit vor, bei der es um die Entwicklung und Konstruktion einer
Energiegewinnungsvorrichtung für die neue Generation von Herzschrittmachern
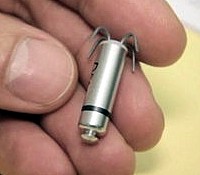
geht: miniaturisierte Implantate ohne Batterien, die aufgrund
ihrer Länge von 24 mm und Dicke von 9 mm über die Vene in die Herzkammern
eingeführt und direkt am Herzmuskel angebracht werden können – bislang
aber noch immer Batterien benötigen und daher nach rund zehn Jahren
ausgetauscht werden müssen. Die Arbeit ist im Netz
einsehbar.
Nach Analyse der verschiedenen mechanischen Energiequellen in der Herz-Umgebung und den damit verbundenen Mechanismen zur Energiegewinnung entscheidet sich Deterre für ein Konzept, das auf den regelmäßigen Blutdruckänderungen beruht. Er gestaltet ein Implantat in einer flexiblen Verpackung, welches die Kräfte des Bluts auf einen internen Wandler überträgt.
Hierfür werden hochflexible, 10 µm dünne Blasebälge aus Metall entwickelt, hergestellt und getestet. Die Prototypen, die sich als Implantatverpackung unter Blutdruckwirkungen verformen, bestätigen das vorgeschlagene Konzept.

von Deterre
Durch Konstruktionsanalyse, numerische Simulationen, Prototypenfertigung und experimentelle Tests werden zudem piezoelektrische Spiral-Wandler mit optimiertem großen Hub einschließlich ihrer komplexen Elektroden-Muster untersucht. Alternativ entwickelt Deterre einen neuen elektrostatischen Wandler, der in 3D-Bauweise eine mehrschichtige Überlappungsstruktur mit ineinandergreifenden Kämmen aufweist und vielversprechende numerische Ergebnisse zeigt.
Experimentell wird bislang eine Leistungsdichte von 3 µJ/cm3 pro Zyklus erreicht, doch bei entsprechender Weiterentwicklung sollte die Vorrichtung genügend Energie liefern, um die neuen Herzschrittmacher selbstständig und praktisch fortwährend mit Strom versorgen zu können. Die Vorteile gegenüber anderen internen Energiefängern sind in erster Linie die höhere Leistungsdichte, die Anpassungsfähigkeit an Änderungen der Herzschlagfrequenz und das hohe Miniaturisierungspotential. Gemeinsam mit Elie Lefeuvre hatte Deterre bereits 2012 ein EU- und ein US-Patent angemeldet (EP-Nr. 2520333; US-Nr. 20120283807).
Deterres im Netz veröffentlichte Doktorarbeit trägt den Titel ‚Toward an energy harvester for leadless pacemakers‘, ein parallel erschienener wissenschaftlicher Artikel ist unter ‚Micro Blood Pressure Energy Harvester for Intracardiac Pacemaker‘ zu finden. Es läßt sich aber nichts darüber finden, daß die Technologie später weiter vorangetrieben wurde – oder daß die Patente jemals umgesetzt wurden.
Im
Januar 2014 stellt eine von Prof. John
A. Rogers an der University of Illinois at Urbana–Champaign (UIUC)
geleitete Gruppe, an der auch Kollegen der Tsinghua
University in
China mitarbeiten, ein implantierbares flexibles, piezoelektrisches
Kleingerät vor, das die mechanische Energie eines schlagenden
Herzens erntet. Der ausführliche und
im Netz einsehbare Artikel von Rogers et al. trägt den Titel ‚Conformal
piezoelectric energy harvesting and storage from motions of the heart,
lung, and diaphragm‘.

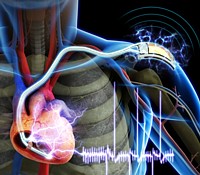
Das neue Gerät enthält einen Film, der aus 500 nm dünnen Bändern aus Blei-Zirkonat-Titanat (PZT) mit Gold- und Platinelektroden besteht, die von einem flexiblen, biokompatiblen Kunststoff umhüllt sind. Ärzte können das Nanoband-Gerät direkt an das Herz, die Lunge oder das Zwerchfell des Patienten nähen. Wenn sich die Körperteile bewegen, werden die Bänder leicht verbogen und erzeugen geringe Mengen an Strom.
Bei Tests an Kühen und anderen großen Tieren kann genügend Energie produziert werden, um einen Schrittmacher oder andere implantierbare Geräte auf unbestimmte Zeit mit Strom zu versorgen. Klinische Studien an Menschen sollen erst erfolgen, wenn Langzeittests belegt haben, wie lange die Geräte innerhalb des Patienten überleben können. Zudem will das Rogers-Team zuvor noch einen Ersatz für das Blei finden, um so nahe an lebenswichtigen Organen keine toxische Substanz plazieren zu müssen.
Rogers ist überhaupt äußerst aktiv, so gründete er u.a. im Jahr 2005 als Spin-off die Firma Semprius Inc. zur Entwicklung kostengünstiger und leistungsstarker CPV-Module, sowie 2008 die Firma MC10 Inc., die sich mit thermoelektrischen Generatoren beschäftigt. 2010 arbeitet er dann an Wegen, um Solarzellen-Silizium durch günstigeres Galliumarsenid und andere Halbleiterverbindungen zu ersetzen, und 2011 vermeldet ein von ihm geleitetes internationales und interdisziplinäres Teams die Entwicklung einer elektronischen Haut, die mittels integrierter Solarzellen durch Licht betrieben wird. Eine weitere Beschäftigung mit dem piezoelektrischen Herzschrittmacher läßt sich aber nicht belegen.
(Grafik)
Im Juni 2014 folgt eine Meldung, der zufolge auch
eine Forschergruppe in Südkorea einen Herzschrittmacher entwickelt
habe, welcher durch die Nutzung von Energie aus den körpereigenen
Muskeln so gut wie dauerhaft angetrieben werden kann. Auf
einer Grafik wird gezeigt, wie dies beispielsweise am Schultergelenk
geschehen könnte.
Das Forschungsteam um Prof. Keon Jae Lee vom Korea Advanced Institute of Science and Technology (KAIST) und Prof. Boyoung Joung vom Severance-Krankenhaus der Yonsei University hat einen flexiblen piezoelektrischen Nanogenerator geschaffen, der verwendet wird, um das Herz einer lebenden Ratte direkt zu stimulieren – mit elektrischer Energie, die aus kleinen Körperbewegungen des Tieres produziert wird.
Basierend auf früheren Experimenten des KAIST zur Herstellung preiswerter, großflächiger Versionen dieser Technologie (s.u. Piezoelektriztät, 2012), erstellt das Team den neuen flexiblen Hochleistungs-Nanogenerator aus einem Dünnfilm-Halbleitermaterial namens Bleimagnesiumniobat-Bleititanat (PMN-PT), anstatt aus Graphenoxid und Kohlenstoffnanoröhrchen, wie bei vorherigen Versionen. Als Ergebnis kann das Gerät aus kleinen Biegebewegungen des Nanogenerators bis zu 8,2 V und 0,22 mA elektrische Energie ernten. Die auf diese Weise erzeugte Spannung und der Strom sind von ausreichender Menge, um das Rattenherz direkt zu stimulieren.
Zu erwähnen ist an dieser Stelle eine Art Vorläufer, der auf Asher
Holzer aus Haifa und die im Jahr 2004 gegründete
israelische Firma Sirius Implantable Systems Ltd. mit
Sitz in Hefer zurückgeht. Bereits 2005 wird von
diesen das Patent für ein Mikrogenerator-Implantat beantragt, das
einen piezoelektrischen Wandler verwendet, welcher direkt neben sich
bewegenden Organen plaziert wird (US-Nr. 20050256549, veröffentlicht 2005).
Das Systeme soll auch schon an Tieren getestet worden sein.
2009 meldet das Unternehmen noch ein ,High efficiency piezoelectric micro-generator and energy storage system’ an, als dessen Erfinder Arieh Meitav und Dan Gelvan genannt werden (US-Nr. 20110304240, veröffentlicht 2011; vgl. EP-Nr. 2379166), doch später hört man nichts mehr darüber.
Um im Kontext zu bleiben, sollen an dieser Stelle auch ähnliche Entwicklungen
im Laufe der Folgejahre erwähnt werden.
Dazu gehört ein im September 2016 erscheinender Bericht von Wissenschaftler der Johns Hopkins University und der Universität Bonn, die in Tests an Mäusen und Simulationen des menschlichen Herzens herausgefunden haben, daß schmerzfreie Lichtimpulse die normale Herzfunktion wiederherstellen können und damit möglicherweise den Weg zu implantierbaren optischen Defibrillatoren ebnen, die bei gefährlichen Herzrhythmusstörungen eine sanfte und sichere Alternative zu einem harten Elektroschock darstellen.
(Grafik)
Im Februar 2019 werden gleich zwei Studien veröffentlicht,
die sich mit dem Herzschlag beschäftigen. Zum einen
sind dies Forscher der Thayer School of Engineering in
Dartmouth, die zusammen mit Medizinern der Universität von
Texas in San Antonio eine Kombination aus Dünnschicht-Energieumwandlungsmaterialien
und einem minimal invasivem mechanischem Design untersuchen (‚Energy
Harvesting: Flexible Porous Piezoelectric Cantilever on a Pacemaker
Lead for Compact Energy Harvesting‘).
Das Team um Prof. John X. J. Zhang hat das Ziel, sich selbst aufladende Batterien für eine potentiell breite Palette von implantierbaren Geräten wie Herzschrittmacher und Defibrillatoren zu entwickeln. Hierzu wird ein marktüblicher Herzschrittmacher modifiziert, so daß die kinetische Energie, die das schlagende Herz auf die Elektrode des Herzschrittmachers ausübt, den Piezoeffekt nutzt, um die Batterie kontinuierlich wieder aufzuladen.
Das dabei eingesetzte Material ist eine piezoelektrische Spezialfolie aus einem Polymer namens PVDF. In porösen Strukturen ausgeführt – entweder als Reihe kleiner Bündel oder als flexibler Ausleger –, kann sie mechanische Bewegungen in Strom umwandeln. Die erste Runde der Tierversuche wird mit „hervorragenden Ergebnissen“ abgeschlossen, die in Kürze veröffentlicht werden sollen.
Die zweite Studie trägt Titel ‚Direct Powering a Real Cardiac Pacemaker
by Natural Energy of a Heartbeat‘ und geht auf Hao Zhang, Bin
Yang und ihre Kollegen der Second Military Medical
University und der Shanghai Jiao Tong University zurück.
In diesem Fall besteht der Generator aus einem elastischen Skelett und zwei piezoelektrischen Kompositen, die in vivo einen hohen Ausgangsstrom von 15 μA erzeugen können und bereits erfolgreich einen voll funktionsfähigen Herzschrittmacher versorgen, der ein Schweineherz durch die Nutzung der natürlichen Energie des Herzschlags ohne externe Energiespeicherelemente antreiben kann.
Winzige Roboter, der sich im menschlichen Körper bewegen, werden im
März 2019 von Wissenschaftlern des Dartmouth
College und der City University of Hong Kong um
Prof. Zi Chen und Peng Shi vorgestellt
(‚A Remotely Controlled Transformable Soft Robot Based on Engineered
Cardiac Tissue Construct‘).
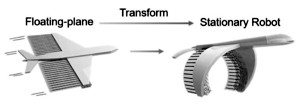
(Grafik)
Die 3D-gedruckten, biohybriden Roboter sind mit einer Schicht Herzzellen bedeckt, während ihre Flügel mit einem lichtempfindlichen Hydrogel beschichtet sind.Wenn die Zellen im Gleichschritt schlagen, bewegen sie den flexiblen Schwanz wie eine Walflosse auf und ab, was bewirkt, daß sich der Roboter durch eine flüssige Umgebung vorwärts bewegt. Dabei sorgen die ausgeklappten Flügel für Auftrieb – und sie bleiben ausgeklappt, solange sich das Gerät in einer dunklen Umgebung befindet.
Wird das Gel auf den Flügeln jedoch mit hautdurchdringendem Nahinfrarotlicht bestrahlt, verändert es seinen Zustand und bewirkt, daß sich die Flügel nach unten rollen. Dies verringert den Auftrieb und erzeugt gleichzeitig einen Widerstand, der die Vorwärtsbewegung des Geräts behindert und z.B. die Freisetzung der Medikamentenladung an einer bestimmten Stelle ermöglicht. Die Herzmuskelzellen arbeiten weiter, sind aber nicht in der Lage, die Bremskraft der Flügel zu überwinden.
In Labortests wird der Roboter bereits erfolgreich für die gezielte Verabreichung von Medikamenten gegen Krebszellen eingesetzt. Die Forscher arbeiten nun an einem System, mit dem sie jeden Flügel einzeln einrollen können, um die Manövrierfähigkeit des Geräts zu erhöhen.
Im April 2019 erscheint ein Bericht von Zou
Li, Han Ouyang und ihren Kollegen am Beijing
Institute of Nanoenergy and Nanosystems der Chinesischen Akademie
der Wissenschaften (‚Symbiotic cardiac pacemaker‘, im Netz einsehbar).
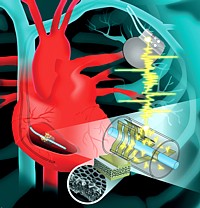
Hierin wird beschrieben, wie ein triboelektrischer
Generator (TENG) nahe des Herzens eingesetzt
werden, um bei Druck oder Verformung Strom zu erzeugen: Beim Kontakt
zweier Materialschichten kommt es zum Austausch von Elektronen, die
bei der anschließenden Trennung abgeleitet werden können.
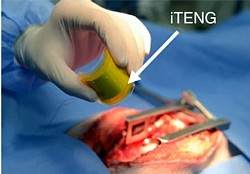
des TENG
Konkret besteht der Energiesammler aus einer triboelektrischen Schicht polarisierten Polytetrafluorethylens (PTFE) und einer Aluminiumschicht, die als Elektronendonor fungiert. Beide Schichten sind durch einen porösen, schwammartigen Abstandshalter getrennt. Durch die Herzbewegung wird diese elastische Trennschicht zusammengedrückt, es kommt zum Elektronentransfer, die erzeugte Spannung wird über eine Elektrode abgeleitet und an einen kleinen Kondensator als Speichereinheit übertragen.
Der gesamte symbiotische Generator ist in einer Hülle eingeschlossen und kann so zusammen mit dem Schrittmacher und der Speichereinheit in den Brustkorb implantiert werden. Dies wird erfolgreich an Schweinen getestet, bei denen der triboelektrische Energiesammler nahe an der Wand der linken Herzkammer implantiert wird. Bei jeder Systole des Herzens wird der Generator zusammengedrückt und erzeugt einen Spannungspuls, dessen Energie rund 0,495 µJ entspricht. Im Laufe von drei Stunden steigt dadurch in der Speichereinheit die elektrische Spannung schrittweise von 0 auf 3,55 V.
In Tests absolviert der gut verträgliche und haltbare triboelektrische Generator bereits mehr als 100 Millionen mechanische Stimulationszyklen und stellt damit eine der vielversprechendsten Methode dar, um biomechanische Energie in vivo zu sammeln.

Herzpflaster
Wie im November 2020 berichtet wird, arbeitet ein
Team der University of Houston ebenfalls an der Energiegewinnung
aus dem schlagenden Organ (‚An epicardial bioelectronic patch made
from soft rubbery materials and capable of spatiotemporal mapping of
electrophysiological activity‘).
Die Forscher um Prof. Cunjiang Yu haben demnach ein gummiartiges Pflaster entwickelt, das biegsam genug ist, um auf ein schlagendes Herz geklebt zu werden, und das dank der flexiblen Elektronik eine ganze Reihe von Sensorfunktionen enthält. Frühere implantierbare Herzgeräte waren dagegen oft zu starr, um sich beim Schlagen des Herzens mitzubewegen, was das Gewebe belasten kann.
Aufbauend auf ihren früheren Arbeiten, bei denen flexible Elektronik in Roboterhände und dehnbare Häute integriert wurde, konstruieren die Forscher ein Herzpflaster, das der mechanischen Weichheit des Herzgewebes entspricht. In das Pflaster werden Sensoren eingepflanzt, die Daten zu elektrophysiologischer Aktivität, Belastung, Temperatur und Herzschlag an mehreren Stellen des Organs gleichzeitig erfassen.
Das Herzpflaster wird erfolgreich an Schweineherzen getestet, wobei auch demonstriert werden kann, wie das Gerät sich selbst mit Energie versorgt, indem es Energie aus dem schlagenden Organ gewinnt.
Im Bezug auf implantierbare Pflaster, die zur Behandlung geschädigter
Herzen eingesetzt werden, sei auf eine im Februar 2020 erschienene
Studie des Trinity College Dublin verwiesen, wo
Prof. Michael Monaghan und seine Kollegen das Problem
angegangen sind, daß nach einem Herzinfarkt ein Teil des schlagenden Herzgewebes durch
nicht schlagendes Narbengewebe ersetzt wird, was die Funktion des
Herzens dauerhaft beeinträchtigt (‚Electroconductive Melt Electrowritten
Patches Matching the Mechanical Anisotropy of Human Myocardium‘).
Das neues Pflaster soll an der Außenseite des Herzens angebracht werden und den Bereich mit Narbengewebe überbrücken. Es besteht aus einem medizinisch zugelassenen dehnbaren Polymer und ist mit einem Netz aus einem separaten elektrisch leitfähigen Polymer namens Polypyrrol beschichtet.
Nach der Implantation soll das Pflaster die elektrischen Signale der umliegenden Herzzellen aufnehmen und über den Spalt weiterleiten und sich im Takt mit ihnen ausdehnen und zusammenziehen. Bislang wurde es an isolierten biologischen Gewebestücken getestet, Tierversuche sollen folgen.
Zum Hintergrund: Es gibt bereits andere experimentelle Herzpflaster, die die gleiche Funktion erfüllen: Im Jahr 2011 erschienen beispielsweise entsprechende Berichte der Brown University in Rhode Island und des Indian Institute of Technology Kanpur, wo ein elektrische Impulse übertragendes Pflaster aus Kohlenstoff-Nanofasern entwickelt wird, das mit lebenden Herzzellen besiedelt wird – sowie des Massachusetts Institute of Technology (MIT), wo die Herzzellen eine schwammartige Matrix aus Alginat besiedeln, dem eine Lösung beigemischt wird, die Milliarden winziger Goldnanodrähte enthält, welche die Lücken zwischen den Zellen überbrücken.
Im Jahr 2016 folgen Berichte über ähnliche Arbeiten an lebensfähigen bionischen Herzpflastern an der Universität Tel Aviv (TAU), und 2017 melden Experten der University of Minnesota und der University of Alabama-Birmingham, daß sie ein neues Pflaster entwickelt haben, das eine vollständigere Heilung des Herzens ermöglicht. Hier wird das Pflaster aus herzspezifischen Strukturproteinen im 3D-Bioprintverfahren Form einer gerüstartigen Matrix hergestellt, die anschließend mit aus Stammzellen gewonnenen Herzzellen besiedelt wird.
Da es sich jedoch in allen diesen Fällen nicht um eine energetische Nutzung handelt, sollen sie hier nicht weiter vertieft werden.
Weiter mit den muskulären Systemen...